Dez razões pelas quais as pessoas deixam de frequentar o tratamento do HIV na Zâmbia
RETENÇÃO E LIGAÇÃO PARA OS CUIDADOS
As relações entre o paciente e o provedor são prejudicadas por más condições de trabalho e aplicação rígida de modelos uniformizados de atendimento, de acordo com uma investigação detalhada de porquê as pessoas com HIV abandonam os serviços de tratamento de HIV na Zâmbia, recentemente publicadas no BMJ. Saúde global. Mas os pacientes classificam os serviços anti-retrovirais mais do que os curandeiros tradicionais, que percebem ter problemas próprios.
O estudo identificou tanto desafios estruturais (incluindo recursos, instalações clínicas e diretrizes clínicas) quanto questões de pessoal (incluindo atitudes e práticas de trabalho discricionárias) que desencorajavam as pessoas a permanecerem nos serviços de HIV. A falha dos serviços de saúde em manter as pessoas vivendo com o HIV envolvidas em tratamentos e cuidados ao longo da vida tem sérias implicações para a saúde individual e da população.
Chanda Mwamba e colegas do Centro de Pesquisa de Doenças Infecciosas na Zâmbia procuraram pacientes que foram “perdidos para o acompanhamento” para perguntar-lhes sobre sua experiência pessoal durante o acesso aos cuidados. Eles conduziram entrevistas em profundidade com 69 pacientes de 12 instalações em quatro províncias. Os pesquisadores asseguraram que recrutassem participantes de quatro grupos – pacientes atualmente engajados no cuidado do HIV, desengajados dos cuidados e pacientes que haviam sido transferidos para outra instituição, bem como os parentes próximos de pacientes que haviam morrido.
Além disso, 158 profissionais leigos e profissionais de saúde participaram de 24 discussões em grupos focais. Por fim, os pesquisadores observaram práticas de trabalho em cada unidade de saúde por dois dias cada, a fim de entender melhor os fluxos de trabalho e as interações humanas.
As seguintes citações de pacientes e profissionais de saúde ilustram dez razões pelas quais as pessoas acham que o envolvimento contínuo com o cuidado é um desafio.
- As unidades sanitárias , muitas vezes estão muito longe das casas das pessoas, especialmente para aquelas em áreas rurais. As visitas às unidades sanitárias custam aos pacientes tempo e dinheiro. “Então, nós dois temos esse vírus. Mas fui eu quem cuidou do meu marido. Eu colecionei o remédio dele também. Mas eu estava sozinha cuidando dele em casa. E foi demais para mim porque tivemos datas diferentes. Foi assim que parei … não teria transporte. Eu teria que andar. Eu não consegui .”
- Alta demanda da unidade sanitária, não protege suficientemente a privacidade dos pacientes. “Quando um indivíduo vai à unidade sanitária, tem pessoas … Eles vão ver o que acontece lá na no sector de tratamento antirretroviral para que possam vir e dizer às pessoas o que está acontecendo. E é isso que me faz sentir preguiçoso [ir para o atendimento] ”.
- A eterna falta de pessoal aumenta o tempo de espera. “Eu me transferi porque … meu marido disse que é muito congestionado. Nós tentamos ir lá no outro dia. Estava congestionado. Eram muitas pessoas. Nós esperamos e nos cansamos e ele disse: “Não! Este lugar não é propício para nós! Talvez, vamos [em outro lugar] ‘.
- A equipe freqüentemente abre as clínicas com atraso ou fecha-as cedo, criando congestionamento. “Quando se trata de abrir a clínica, eles geralmente estão atrasados. Eles podem abrir às 08:00, mas para eles começarem a trabalhar, eles normalmente atrasam. Você vai descobrir que eles vão começar às 09:00 ou 10:00 e então você já estará cansado de esperar. Então isso dificulta. ”
- Registros médicos são freqüentemente perdidos ou alterados, exigindo testes extras e mais espera. “A maneira como eles mantêm os arquivos, o arquivo foi perdido diariamente. Quando cheguei, todas as vezes, o arquivo foi perdido! ”
- Visitas clínicas para pegar medicação são muito freqüentes e são inflexíveis. “Eu sou um pedreiro. Uma vez ou até três vezes eu disse a eles: “Vou trabalhar e não sei quando posso voltar. De modo que um mês [de drogas] você está me dando, melhor você me dá por três meses. ”Mas eles se recusaram dizendo: ‘É o nosso programa, então é melhor darmos a você algo por um mês’. essas pessoas não pensaram em mim. ”
- Os pacientes que perderam consultas são frequentemente selecionados para ter visitas ainda mais frequentes, sem abordar as razões pelas quais a pessoa acha difícil comparecer. “Quando um paciente perdeu uma consulta por vários dias, nós – não é um castigo no sentido real -, mas punimos o cliente quando ele volta. Em vez de dar a esses pacientes drogas que durariam talvez três meses, damos a eles drogas para durar duas semanas, para que possam se acostumar a lembrar com frequência que precisam ir à unidade sanitária.”
- Alguns profissionais de saúde são considerados ineficientes ou pouco profissionais. “Do jeito que eles fazem as coisas, essa é a nossa grande queixa! Mesmo quando o médico chegar, eu direi ao médico: “Essas pessoas, se não puderem administrar esses empregos, devemos ajudar, porque podemos gerenciar colocando os arquivos em ordem para que, quem vier, saibamos onde estão as coisas!”
- Alguns funcionários revelam o estado de HIV dos pacientes ou não protegem suficientemente sua confidencialidade. “Isso não acontece com frequência, mas tenho observado várias vezes sozinho, talvez até mesmo o tenha feito. Mas é outra coisa que tira os clientes, porque quando começamos a lidar com eles, prometemos a eles que vamos manter as informações confidenciais. ”
- Alguns profissionais de saúde intimidam ou humilham os pacientes que chegam atrasados ou fazem solicitações que são consideradas irracionais. “Quando você vai [para a unidade sanitária ] e faz [perguntas], eles gritam com você. Mas eles não devem gritar para nós. Em vez disso, eles deveriam encorajar essa pessoa … Mas, só para dizer a verdade, uma das razões pelas quais parei de cuidar é porque eles nos gritam muito – eles são rudes! ”
Os pesquisadores dizem que suas descobertas mostram a necessidade de mais recursos, treinamento e orientação para serviços de HIV e seus trabalhadores na Zâmbia. Os modelos de serviços de saúde devem ser reprojetados para incentivar os profissionais de saúde a fornecer cuidados centrados no paciente e exercitar a flexibilidade para atender às diferentes necessidades e circunstâncias dos pacientes.
Tratamentos alternativos
O estudo também mostrou que os pacientes veem a terapia anti-retroviral e os serviços do Ministério da Saúde como mais eficazes e de melhor qualidade do que os tratamentos dos curandeiros tradicionais. Esta notícia encorajadora está em contraste com alguns estudos anteriores.
As pessoas sentiram que os testes de diagnóstico médico e os resultados forneceram a base para um tratamento mais confiável e direcionado:
“É diferente [com um curandeiro tradicional], porque esse não explica a você o que está doendo ou como vai funcionar com o remédio que ele lhe dará.”
“Estes [ARVs] estão funcionando. Eu não fui para outro lugar para um curandeiro tradicional porque esse medicamento não faz nada. ”
Enquanto os serviços do Ministério da Saúde são gratuitos, os curandeiros tradicionais recebem o dinheiro das pessoas sem entregar os resultados prometidos.
“Mmmmmm, o curandeiro tradicional só pode terminar seu dinheiro. Mas na clínica não há nada pago, é grátis. ”
Referência
Mwamba C, et al. “Eles se importam rudemente!”: Fatores de recursos e sistemas de saúde relacionais que influenciam a retenção de pessoas que vivem com HIV na Zâmbia. BMJ Global Health 2018; 3: e 001007. (Texto completo disponível gratuitamente).
PREVENÇÃO DA TRANSMISSÃO VERTICAL MÃE-FILHO DO HIV
Supressão viral chave para prevenir a transmissão de mãe para filho, mas a insegurança alimentar, tuberculose e ITS também podem ser fatores de risco.
A redução da carga viral materna durante a gravidez é o factor mais importante na prevenção da transmissão mãe-filho (MTCT) do HIV, confirmam os resultados de um grande estudo publicado no The Pediatric Infectious Disease Journal. Outros factores de risco para transmissão vertical incluíram alimentação insuficiente, uma infecção sexualmente transmissível recente (ITS) e um histórico de doenças associadas à imunossupressão.
A pesquisa foi realizada no Malawi e envolveu mulheres que não fizeram terapia anti-retroviral (TARV) até o início do parto. A taxa de transmissão foi de 0,5% entre mulheres com carga viral abaixo de 1000 cópias/ml, comparativamente a 7,5% entre mulheres com carga viral acima de 10 000 cópias/ml.
“Nosso estudo confirma que, com a supressão da carga viral materna a maioria dos casos de transmissão vertical perinatal pode ser evitada”, comentam os autores. “Estas descobertas podem ajudar a informar as decisões para populações alvo de programas que visam melhorar a cobertura de TARV durante a gravidez, e podem apoiar esforços para reconhecer e tratar a tuberculose materna, ITS e outras infecções antes e durante a gravidez, e esforços para melhorar o estado nutricional materno no período pré-natal, para alcançar a eliminação mundial da infecção pediátrica pelo HIV e melhorar os resultados para as mulheres grávidas infectadas pelo HIV. ”
Estima-se que 150.000 crianças com 15 anos ou menos foram infectadas com HIV em 2015, principalmente devido à transmissão vertical mãe – filho (TVMF). Transmissões de mãe para filho podem ocorrer no útero, no momento do parto ou devido à amamentação. TARV durante a gravidez e parto reduz drasticamente o risco de TVMF. No entanto, apesar dos aumentos maciços na cobertura de TARV, em 2014, estima-se que 25% das mulheres grávidas com infecção pelo HIV conhecida não receberam TARV.
Além disso, como um grande número de mulheres soropositivas não recebe TARV durante a gravidez, é importante identificar todo o espectro de factores de risco para a transmissão vertical. Pesquisadores do estudo Amamentação, Antirretrovirais e Nutrição (BAN) realizaram uma análise retrospectiva dos registros de 2275 mulheres grávidas soropositivas.
O recrutamento e o acompanhamento ocorreram entre 2004 e 2010. Os participantes precisavam ter pelo menos 14 anos de idade, não ter recebido TARV, estar planejando amamentar e ter uma contagem de células CD4 de pelo menos 250 células / mm3. As mulheres não receberam nenhum TARV até o início do trabalho de parto, quando as mães e os bebês receberam uma dose única de nevirapina. Todas as mães também receberam zidovudina e lamivudina duas vezes ao dia desde o início do trabalho de parto e durante sete dias após o parto, com todas as crianças recebendo zidovudina e lamivudina ajustadas ao peso duas vezes ao dia por sete dias.
Os bebês foram testados para o HIV através de DNA PCR no nascimento e novamente nas semanas um, dois e quatro após o parto.
Aproximadamente um terço das mulheres tinha uma contagem de células CD4 abaixo de 350 células / mm3 e 63% tinham uma carga viral acima de 10.000 cópias/ml durante a gravidez. Apenas 35% tinham um nível maior do que educação primária. Anemia durante a gravidez, insegurança alimentar e má nutrição eram comuns e observadas em mais de 40% dos participantes.
Houve 119 casos de TVMF, com 115 ocorrendo no útero, os quatro casos restantes nas duas primeiras semanas de vida.
As mulheres que transmitem o HIV aos seus filhos tiveram cargas virais medianas significativamente mais elevadas durante a gravidez do que as mulheres que não transmitiram (61.830 cópias/ml versus 16.529 cópias/ml, p <0,001).
Das 200 mulheres que tiveram uma carga viral abaixo de 1.000 cópias/ml durante a gravidez, houve apenas um caso de transmissão vertical, uma taxa de transmissão de 0,5%. É digno de nota que havia uma história de infecção materna por tuberculose neste caso. A taxa correspondente para mulheres com cargas virais entre 1.000 cópias/ml e 10.000 cópias/ml foi de 1,4%, aumentando para 7,5% para mulheres com carga viral superior a 10.000 cópias/ml.
As mulheres que transmitem o HIV aos seus bebés também tinham maior probabilidade de ter uma contagem de células CD4 abaixo de 350 células/mm3 (36% vs 30%) do que as mulheres não transmissoras.
A escassez de alimentos foi mais comum entre as mães transmissoras do que as mães que não transmitiram (51% vs 41%). Uma história de TB foi mais prevalente entre os transmissores do que não transmissores (6,7% vs 2,8%), assim como a história de herpes zoster (14% vs 4%). Os transmissores tinham menos probabilidade de ter qualquer educação pós-primária formal do que os não transmissores (25% vs 35%).
Os pesquisadores observam que, embora a insegurança alimentar possa ser uma causa de deficiências nutricionais, estudos randomizados anteriores de suplementos nutricionais não se mostraram eficazes. É possível que a escassez de alimentos neste estudo tenha funcionado como um indicador dos determinantes sociais da saúde. Eles especulam que as histórias de tuberculose e herpes zoster podem ter causado imunossupressão e aumentos breves e não observados nas cargas virais. As ITS podem estar associadas à disseminação genital do HIV.
“Claramente, todo esforço deve ser feito para iniciar a TARV e reduzir a carga viral em gestantes infectadas pelo HIV”, concluem os autores. “Nossos dados também sugerem que a insegurança alimentar, a história de doenças que indicam imunossupressão e a história de outras ITS podem ser fatores de risco para a transmissão vertical perinatal.”
Referência
Ewing AC et al.; Preditores da transmissão perinatal do HIV entre mulheres sem terapia antirretroviral prévia em um contexto de recursos limitados: o estudo BAN. O Jornal de Doenças Infecciosas Pediátricas, edição on-line, DOI: 10.1097 / INF.0000000000002220 (2018).

CARGA VIRAL INDETECTAVEL E TRATAMENTO COMO PREVENÇÃO
Risco “insignificante” de transmissão do HIV com uma carga viral suprimida, informam oficiais de saúde pública canadense. O potencial de transmissão sexual do HIV quando uma pessoa que vive com HIV adere à terapia antiretroviral e mantém uma carga viral indetectável é “insignificante”, diz a Agência de Saúde Pública do Canadá, em uma revisão feita para o Departamento de Justiça do país. Além disso, o risco de transmissão é “baixo” quando uma pessoa vivendo com o VIH está a tomar terapêutica anti-retroviral sem carga viral ou indetectável inferior a 200 cópias / ml, sendo utilizados preservativos ou ambos.
Espera-se que esta confirmação da evidência científica ajude a reduzir a criminalização da não divulgação, que é generalizada no Canadá. As pessoas podem ser processadas por não revelarem o seu estado seropositivo quando se envolvem em actividades sexuais que representam uma “possibilidade realista” de transmissão do HIV.
A Agência de Saúde Pública do Canadá realizou uma revisão sistemática, a fim de identificar as revisões existentes e estudos que forneceram dados para calcular um risco absoluto de transmissão sexual do HIV entre parceiros sexuais de diferentes status de HIV.
Estudos publicados até abril de 2017 foram incluídos. Como os autores reconhecem, isso significa que alguns dos dados recentes mais importantes, dos estudos PARTNER 2 e Opposites Attract, não estão incluídos. Como não ocorreram transmissões de HIV em pessoas com cargas virais indetectáveis nesses estudos, adicionar seus dados simplesmente acrescentaria à nossa certeza com a qual podemos dizer que a transmissão do HIV não ocorre nessas circunstâncias.
Os autores da revisão analisaram vários cenários.
Cenário 1: O parceiro sexual seropositivo que está a tomar terapêutica anti-retroviral e tem uma carga viral suprimida. Essa estimativa foi baseada nos dados mais antigos dos estudos PARTNER e Opposites Attract, nos quais cargas virais abaixo de 200 cópias / ml foram confirmadas pelo menos a cada seis meses. Não ocorreram transmissões de HIV: 0 transmissões por 1327 pessoas-ano (incidência combinada de 0,00 transmissões / 100 pessoas-ano, IC 95% 0,00-0,28). Os autores dizem que se os dados mais recentes do PARTNER 2 e Opposites Attract fossem incluídos, o intervalo de confiança superior da estimativa seria reduzido (de 0,28 para 0,13), mas a estimativa pontual de 0,00 não mudaria.
Os autores descrevem o risco de transmissão nestas circunstâncias como “insignificante”. Os autores procuraram dados sobre o uso do preservativo nessas circunstâncias, mas não encontraram estudos adicionais. Se um dos parceiros também usou preservativos, o risco também é descrito como “insignificante”.
Cenário 2: O parceiro sexual seropositivo está a tomar terapêutica anti-retroviral (com níveis variados de carga viral). Algumas transmissões de HIV ocorreram nos estudos que foram incluídos: 23 transmissões filogeneticamente ligadas ao HIV em 10.511 pessoas-anos de acompanhamento (incidência combinada de 0,22 transmissões / 100 pessoas-ano, IC 95% 0,14–0,33).
Os autores observam que as pessoas nessas coortes geralmente tinham altos níveis de adesão ao tratamento e altos níveis de supressão da carga viral. Portanto, o potencial de transmissão nessas circunstâncias pode ter sido subestimado.
Cenário 3: O parceiro sexual seropositivo está a tomar terapêutica anti-retroviral (com níveis variados de carga viral) e qualquer dos parceiros usa preservativos. Havia poucas evidências para informar essa estimativa. Os autores baseiam-se em uma revisão sistemática de 2012 que modelou o efeito combinado da terapia anti-retroviral e dos preservativos para derivar os riscos por ato, variando de 0,003 transmissões por mil actos (95% IC 0,00 – 0,03) para sexo vaginal insertivo a 0,11 transmissões por mil actos (IC95% 0,02–0,73) para sexo anal receptivo. Este risco é descrito como “baixo”.
Qualquer um dos parceiros usa preservativos, sem o parceiro seropositivo para o VIH a tomar terapêutica anti-retroviral. Os autores acreditam que as conclusões de uma revisão da Cochrane Collaboration de 2012 ainda fornecem as melhores evidências sobre essa questão. Isto constatou que entre casais sorodiscordantes que relataram “sempre” usar preservativos, havia 1,14 transmissões de HIV por 100 pessoas-ano (IC 95% 0,56–2,04). Os autores canadenses descrevem esse risco como “baixo”.
O Departamento de Justiça do Canadá usou as conclusões deste estudo para elaborar um relatório sobre a resposta do sistema de justiça à revelação do HIV que foi publicado há um ano. Isto declarou: “A lei criminal não deve ser aplicada a pessoas vivendo com HIV que tenham praticado actividade sexual sem revelar sua condição se tiverem mantido uma carga viral suprimida (ou seja, menos de 200 cópias por ml de sangue), porque a possibilidade realista de teste de transmissão não é atendido nessas circunstâncias. ”
Além disso, “o sexo desprotegido com uma pessoa HIV positiva que não revelou seu status não pode mais ser considerado para estabelecer um caso prima facie de não revelação do HIV, já que evidências de tratamento e carga viral serão sempre relevantes para determinar se a possibilidade realista de teste de transmissão é cumprido. ”
No entanto, este importante primeiro passo do governo federal no sentido de limitar a criminalização injusta do HIV não constitui directrizes do Ministério Público, que ainda precisam ser implementadas nos níveis federal e provincial.
Referência
LeMessurier J et al. Risco de transmissão sexual do vírus da imunodeficiência humana com terapia anti-retroviral, carga viral suprimida e uso de preservativo: uma revisão sistemática. CMAJ 2018 19 de novembro; 190: E1350-60. doi: 10.1503 / cmaj.180311

Vacina contra HIV de Harvard oferece um vislumbre de esperança na batalha contra o HIV/SIDA

26 de outubro de 2018, Maputo.
Uma nova vacina para combater o HIV está dando aos profissionais médicos um pouco de optimismo, graças a uma nova pesquisa de Harvard. A vacina contra o HIV produziu uma resposta favorável do sistema imunológico quando testada em 393 pessoas, de acordo com o artigo publicado na revista lancet.
Os testes em humanos vieram de 12 clínicas em todo o mundo, incluindo a África do Sul, a África Oriental, os Estados Unidos e a Tailândia. Todos os participantes foram submetidos a um ensaio duplo-cego, aleatório e controlado por placebo sobre o que está sendo chamado de vacina ‘mosaico’. Os participantes estavam todos entre as idades de 18 a 50 anos, que não tinham HIV e eram saudáveis. Eles receberam quatro vacinas durante o período de 48 semanas.
Todas as combinações de vacina foram consideradas seguras enquanto também produziam a resposta anti-HIV. Além dos testes em humanos, a vacina mostrou uma resposta promissora em 72 macacos rhesus.
“Eu diria que estamos satisfeitos com esses dados até agora, mas temos que interpretá-los com cautela”, disse o co-autor do estudo Dr. Dan H. Barouch, investigador principal do estudo, professor de medicina na Universidade de Medicina de Harvard. e diretor do Centro de Pesquisa em Virologia e Vacinas. “Temos que reconhecer que o desenvolvimento de uma vacina contra o HIV é um desafio sem precedentes, e não saberemos com certeza se esta vacina protegerá os seres humanos”
Este sucesso significa que a vacina pode avançar com o teste. Isso inclui testar a droga em um grupo muito maior de pessoas. Até ao presente momento, é apenas uma das cinco ideias experimentais de vacina contra o HIV-1 a chegar até este ponto em quase quatro décadas da pandemia do HIV.
Mais de 37 milhões de pessoas vivem com HIV ou HIV/SIDA em todo o mundo. Existem quase 2 milhões de novos casos do vírus a cada ano. Enquanto os pesquisadores continuam expandindo o que sabem sobre o vírus e como ele funciona, uma solução e cura a longo prazo permanecem fora de alcance.
Outros pesquisadores advertem, porém, ver esta vacina como a solução final para o vírus. Eles observam que a capacidade de induzir uma resposta imune específica para o HIV não significa que ela evitará que os humanos contraiam o próprio HIV, mas sim o desenvolvimento de uma forte resposta imunológica contra o virus.

Zero transmissão significa risco zero – para casais heterosexuais e de homens que fazem sexo com homens
A probabilidade de uma pessoa que vive com HIV com carga viral indetectável transmitir a infeção ao seu parceiro sexual equivale cientificamente a zero, segundo confirmaram os investigadores do estudo PARTNER na 22ª Conferência Internacional sobre SIDA (IAS) que se realizou de 23 a 27 de Julho em Amesterdão, Holanda.
Os resultados inicialmente apresentados em 2014 correspondentes à fase 1, PARTNER 1, já indicavam , “Indetetável=Intransmissível” (I=I) / “Undetectable=Untransmittable” (U=U), ie, carga viral indectável = ausência de transmissão.Contudo, a certeza estatística deste resultado não foi tão convincente no caso dos homens que fazem sexo com homens ( HSM) ou para o sexo anal , bem como para o sexo vaginal.
O estudo PARTNER recrutou casais serodiscordantes para o HIV (um parceiro a viver com HIV e o outro seronegativo para o HIV) em 14 países europeus. O estudo não encontrou nenhuma transmissão da infeção pelo HIV entre os casais de HSM em que um dos parceiros tenha carga viral abaixo das 200 cópias/ml – apesar de terem ocorrido cerca de 77000 relações sexuais sem o uso do preservativo.
O estudo PARTNER 2 diz-nos que I=I/U=U é tão forte para os HSM (e para o sexo anal) como para os casais heterossexuais.
Referência
Rodger A et al. Risk of HIV transmission through condomless sex in gay couples with suppressive ART: the PARTNER2 study expanded results in gay men. 22nd International AIDS Conference, Amsterdam, abstract WEAX0104LB, 2018.
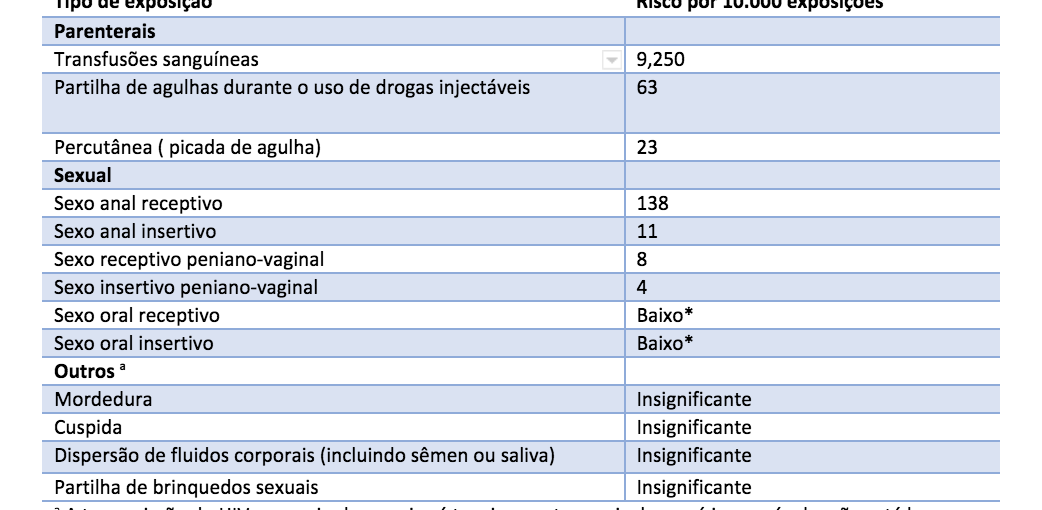
Probabilidade estimada por evento de adquirir HIV de uma fonte infectada, conforme a exposição
| Tipo de exposição | Risco por 10.000 exposições |
| Parenterais | |
| Transfusões sanguineas | 9,250 |
| Partilha de agulhas durante o uso de drogas injectáveis | 63 |
| Percutânea ( picada de agulha) | 23 |
| Sexual | |
| Sexo anal receptivo | 138 |
| Sexo anal insertivo | 11 |
| Sexo receptivo peniano-vaginal | 8 |
| Sexo insertivo peniano-vaginal | 4 |
| Sexo oral receptivo | Baixo* |
| Sexo oral insertivo | Baixo* |
| Outros * | |
| Mordedura | Insignificante |
| Cuspida | Insignificante |
| Dispersão de fluidos corporais (incluindo sêmen ou saliva) | Insignificante |
| Partilha de brinquedos sexuais | Insignificante |
* A transmissão do HIV por meio dessas vias é tecnicamente possível, mas é improvável e não está bem documentada.
Fonte: CDC, www.gov/hiv/policies/law/risk.html; P.Patel: Aids 28:1509, 2014
FALÊNCIA TERAPÊUTICA NO TRATAMENTO DA MALÁRIA
Definição
Febre ou persistência dos sintomas por mais de 3 dias após tratamento correcto e presenca de parasitas exclui-se os gametocitos
Causas
- Vomitos ou diarreia
- Dose insuficiente
- Erro do diagnostic
- Nao cumprimento do tratamento
- Resistencia ao medicamento
- Medicamento de baixa qualidade
- Interações medicamentosas
- Farmacocinetica anormal do individuo
- Imunidade baixa
Se o doente aparecer dentro dos 28 dias após o tratamento com sintomas e esfregaço positivo considerar falência. Tratar segundo a classificação da doença (malária não complicada ou complicada/grave).
Se o doente aparecer após 28 dias do diagnóstico de malária considere como uma nova infecção tratar segundo a classificação da doença (malária não complicada ou complicada/grave).
Fonte: PNCM,2018
AS PRINCIPAIS “MUDANÇAS” DA NORMA DE TRATAMENTO DA MALÁRIA
| Anterior
|
Actual |
| Malária não complicada Artemeter-Lumefantrina (AL) Artesunato-Amodiaquina em dose fixa (ASAQ) Quinino oralMalária complicada/grave Artesunato EV/IM Quinino EV/IM(crianças <5Kg) |
Malária não complicada Medicamento de eleição: Artemeter-Lumefantrina (AL)Medicamento alternativo: Artesunato-Amodiaquina em dose fixa (ASAQ) Quinino oral (mulher grávida no 1º trimestre)Malária complicada/grave Medicamento de eleição: Artesunato EV/IM(incluindo criança com <5kg) Medicamento alternativo: Quinino EV/IM |
| Tratamento pré-referência
Artesunato supositório (APE) Unidade Sanitária Artesunato EV/IM Quinino EV/IM Falência terapêutica Após 14 dias nova infecção
|
Tratamento pré-referência
Artesunato supositório apenas em crianças menores de 6 anos (APE) Unidade Sanitária Artesunato EV/IM Quinino EV/IM Falência terapêutica Antes de 28 dias suspeita falência Após 28 dias nova infecção
|
| Malária na gravidez
Malária não complicada Ø 1° trimestre: Quinino oral Ø 2 ° Trimestre: Artemeter-lumefantrina Malária grave/complicada Ø 1° trimestre: Quinino injectável Ø 2 ° Trimestre: Artesunato injectavel
|
Malária na gravidez
Malária não complicada 1° trimestre: Quinino oral 2 ° Trimestre: Artemeter-lumefantrina Malária grave/complicada Artesunato injectável todos trimestres da gravidez
|
Fonte: PNCM, 2018
TRATAMENTO INTERMITENTE PREVENTIVO DA MALARIA NA GRAVIDEZ
Medicamento recomendado
Comprimidos de Sulfadoxina-pirimetamina 500/25mg
Dosagem e cronologia do TIP
Início (primeira dose) na 13ª semana de gestação
Doses seguintes em intervalos mínimos de quatro semanas até ao momento do parto.
Sulfadoxina/pirimetamina 500 mg/25 mg (SP)
3cp/dose (dosagem total requerida de 1500 mg/75mg)
Toma sob observação directa durante a visita pré-natal (DOT).
Suplemento com sal ferroso e acido fólico(30-60mg) e ac. Fólico 0,4mg(400µg)
MALÁRIA NA GRAVIDEZ – Principais complicações
| Mulher | Feto |
| Anemia grave | Baixo peso a nascença |
| Hiperparasitémia | Atraso do desenvolvimento intra-uterino |
| Hipoglicémia | Prematuridade |
| Edema agudo do pulmão | Abortos espontâneos |
| Malária grave | Morte neonatal |
| Morte materna | Nado morto |