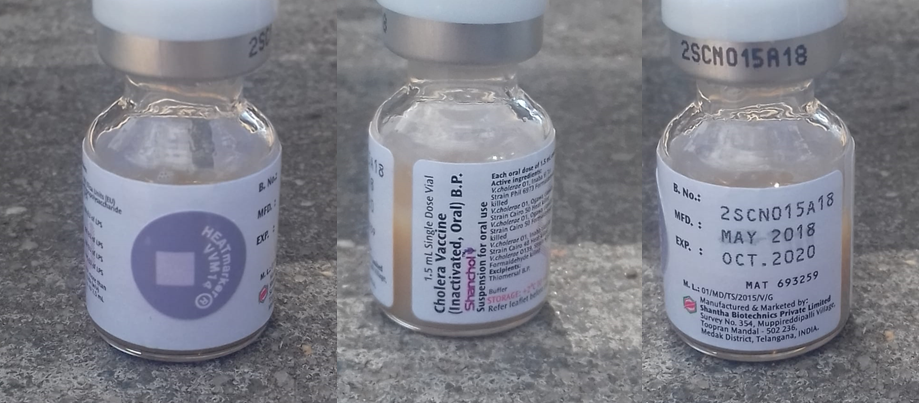
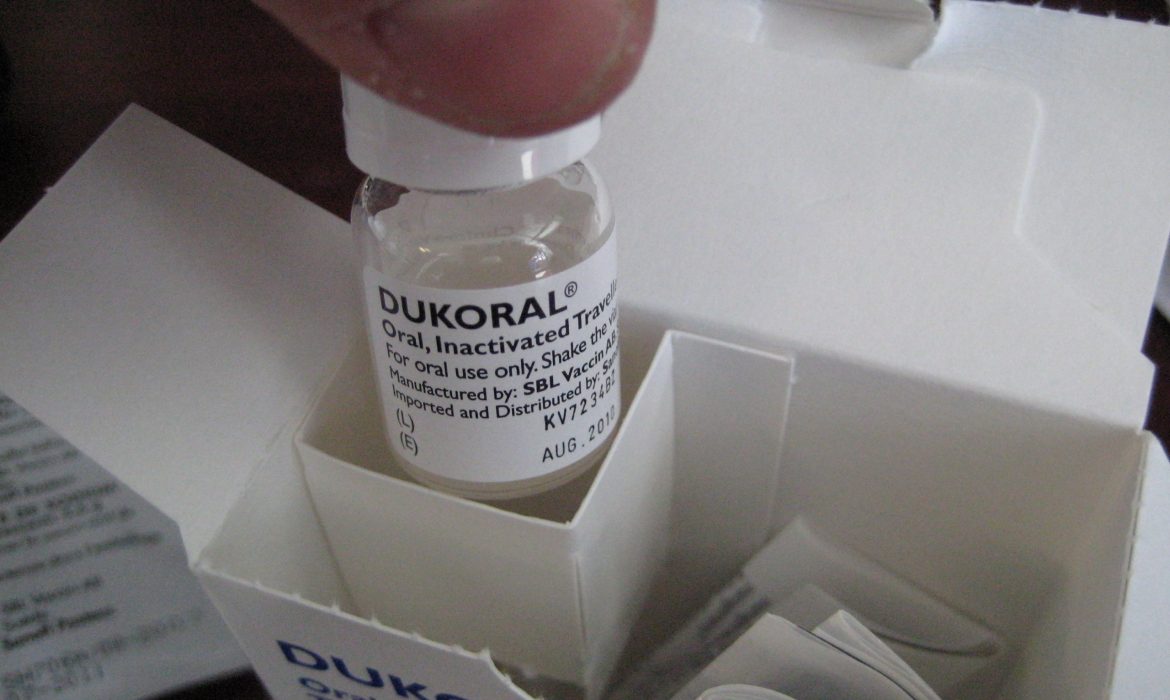
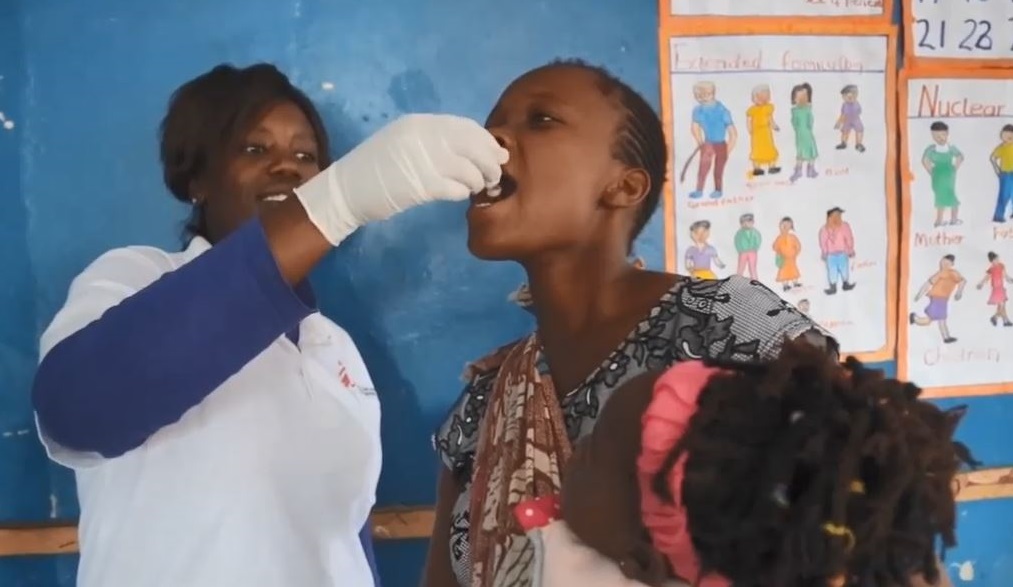
Características do SHANCHOL – Vacina contra à Cólera utilizada na actual Campanha em Sofala Moçambique – Abril 2019
INFORMAÇÃO DE PRESCRIÇÃO
Composição Qualitativa e Quantitativa
Cada dose oral de 1,5 ml contém

INDICAÇÕES TERAPÊUTICAS
Shanchol é indicado para imunização ativa contra o Vibrio cholerae. A vacina pode ser administrada a qualquer pessoa acima de 1 ano de idade. Não estão disponíveis dados para a segurança e eficácia da vacina em bebês (menos de 1 ano de idade). O início mais precoce da proteção pode ser esperado 7-10 dias após a conclusão da série primária da vacina.
POSOLOGIA
A dose recomendada da vacina (1,5 mL) deve ser administrada por via oral. O esquema primário de imunização consiste em duas doses administradas em um intervalo de pelo menos duas semanas. Shanchol não deve ser administrado por via parenteral (intramuscular, subcutânea ou intravenosa). A vacina é recomendada apenas para administração oral.
CONTRA-INDICAÇÕES
Shanchol não deve ser administrado a indivíduos com hipersensibilidade conhecida a qualquer componente da vacina, ou ter apresentado sinais de hipersensibilidade após administração prévia da vacina. O formaldeído é utilizado durante o processo de fabricação e pequenas quantidades podem estar presentes no produto final. Deve ter-se precaução em indivíduos com hipersensibilidade conhecida ao formaldeído. Como com todos os produtos, a possibilidade de reações alérgicas em pessoas sensíveis aos componentes da vacina deve ser avaliada. Tal como com outras vacinas, a imunização com o Shanchol deve ser retardada na presença de qualquer doença aguda, incluindo doença gastrointestinal aguda ou doença febril aguda. Uma doença menor, como uma infecção leve do trato respiratório superior, não é um motivo para adiar a imunização.
ADVERTÊNCIAS E PRECAUÇÕES ESPECIAIS
A vacinação deve ser precedida por uma revisão do histórico médico (especialmente em relação à vacinação prévia e a possível ocorrência de eventos indesejáveis) e um exame clínico. Como com qualquer vacina, a imunização com o Shanchol pode não proteger 100% das pessoas susceptíveis. Esta vacina não é um substituto para a terapia no caso de indivíduos suspeitos de sofrer de cólera ou que apresentem sinais e sintomas de um episódio agudo de doença gastrointestinal ou diarreia aquosa aguda.
Pessoas imunocomprometidas (subsequentes a uma doença ou terapia imunossupressora) podem não obter a resposta imunológica esperada após a vacinação com o Shanchol. Se possível, na opinião do médico, deve ser dada a devida atenção ao adiamento da vacinação até após a conclusão de qualquer tratamento imunossupressor.
Como com todas as vacinas, o tratamento médico apropriado deve estar sempre prontamente disponível no caso de um evento raro de reações anafilácticas após a administração da vacina. Por esta razão, recomenda-se que o vacinado permaneça sob supervisão médica por pelo menos 30 minutos após a vacinação.
POPULAÇÕES ESPECIAIS
HIV/ SIDA
A segurança e a resposta imune do Shanchol não foram avaliadas clinicamente em indivíduos com HIV / AIDS. No entanto, o Shanchol é uma vacina inativada administrada por via oral e age localmente no intestino. Portanto, teoricamente, não se espera que a vacina aumente o risco de cólera em um indivíduo com HIV/ SIDA, mas a vacina pode não provocar a resposta imune esperada e a proteção devido ao estado imunossupressor subjacente.
Gravidez e aleitamento
Não foram realizados estudos clínicos específicos para avaliar a segurança e imunogenicidade de Shanchol em mulheres grávidas ou lactantes e para o feto. A vacina não é, portanto, recomendada para uso durante a gravidez ou durante a lactação. No entanto, o Shanchol é uma vacina morta que não se replica, é administrada por via oral e actua localmente no intestino. Portanto, na teoria, Shanchol não deve representar nenhum risco para o feto humano. A administração de Shanchol a mulheres grávidas ou lactantes pode ser considerada após avaliação cuidadosa dos benefícios e riscos em caso de emergência médica ou epidemia.
População pediátrica
Dados para a segurança e eficácia da vacina em lactentes (menos de 1 ano de idade) não estão disponíveis. A vacina não é, portanto, recomendada para uso em bebês.
REAÇÕES ADVERSAS CONHECIDAS ASSOCIADAS A SHANCHOL
Os seguintes eventos adversos são conhecidos por ocorrerem com o uso de Shanchol. Gastroenterite aguda, diarreia, febre, vômitos, dor abdominal, coceira, erupção cutânea, náusea, fraqueza, tosse, vertigem, secura da boca, úlcera oral (rara), dor de garganta (rara) e amarelecimento da urina (raro). Foi observado que a incidência de eventos adversos é menor após a segunda dose em comparação com a primeira.
MECANISMO DE ACÇÃO
Shanchol consiste em V. cholerae morta. Mostrou-se ser eficaz para administrar a vacina por via oral, o que induz imunidade local. A vacina actua localmente no trato gastrointestinal para induzir uma resposta de anticorpos IgA (incluindo memória) comparável àquela induzida pela própria doença da cólera. Os anticorpos intestinais antibacterianos impedem que as bactérias se liguem à parede intestinal, impedindo assim a colonização de V. cholerae O1 e V. cholerae O139. A proteção contra a cólera é específica tanto para o biótipo quanto para o sorotipo.
EXPERIÊNCIA CLÍNICA
Um estudo duplo-cego, randomizado, placebo controlado foi realizado em Calcutá, na Índia. Um total de 101 (50 vacinas e 51 placebo) adultos saudáveis (homens e mulheres não grávidas) com idades entre os 18 e os 40 anos e 100 (50 vacinas e 50 placebo) crianças e adolescentes saudáveis (homens e mulheres não grávidas) com 1 a 17 anos foram administradas duas doses de Shanchol ou placebo em um intervalo de duas semanas. Após 2 doses de imunização, 53% dos adultos e 80% das crianças vacinadas apresentaram um aumento ≥4 vezes nos títulos séricos de anticorpos vibriocidas do V. cholerae O1. Este estudo mostrou que um regime de 2 doses de Shanchol é seguro, bem tolerado e imunogênico em uma área endêmica de cólera.
Um ensaio de campo controlado por placebo, duplo cego, aleatorizado e controlado foi realizado em Calcutá, na Índia. Este estudo clínico de Fase III foi conduzido para avaliar a eficácia e segurança do regime primário de duas doses de Shanchol em uma área endêmica de Calcutá, na prevenção de diarréia severa por Vibrio cholerae O1 confirmada por cultura e o suficiente para o paciente procurar tratamento em uma unidade de saúde.
Um total de 66.900 indivíduos com idade de um ano ou mais receberam duas doses de Shanchol ou placebo em um intervalo de pelo menos duas semanas. Os sujeitos do estudo foram acompanhados por um período total de cinco anos após a vacinação. Mais de cinco anos de acompanhamento, houve 69 episódios de cólera no grupo da vacina e 219 episódios no grupo placebo. O Shanchol forneceu 65% de proteção contra a infecção clínica por V. cholerae O1 em uma área endêmica por pelo menos cinco anos após a vacinação. A proteção geral foi mantida por 5 anos de acompanhamento.
Não foram detectadas diferenças significativas na proteção vacinal cumulativa de 5 anos entre diferentes grupos etários na vacinação. A proteção das vacinas foi claramente evidente no terceiro a quinto anos de acompanhamento em pessoas vacinadas com cinco ou mais anos de idade e durante o segundo ano em crianças vacinadas em 1-4 anos de idade. Não houve diferenças estatisticamente significativas na ocorrência de eventos adversos relatados entre os receptores de vacina e placebo. Os eventos adversos mais comuns relatados foram diarréia, febre, vômitos e dor abdominal. Este estudo realizado em indivíduos com idade igual ou superior a um ano (sem limite superior de idade), juntamente com os outros estudos não essenciais, formou a base para o licenciamento e a pré-qualificação da OMS da Shanchol.
…
Na Guiné, em 2012, foi organizada a primeira campanha de vacinação em massa usando uma vacina oral contra a cólera de duas doses (Shanchol) como medida de controle adicional para responder à epidemia de cólera em todo o país. Este foi o primeiro uso em larga escala da vacina oral contra a cólera como uma medida de controle de surtos na África; 312.650 doses de vacina foram administradas durante duas rodadas de vacinação em dois distritos costeiros da Guiné. A viabilidade, oportunidade de implementação e custo de entrega foram semelhantes aos de outras campanhas de vacinação em massa. A campanha foi bem aceite pela população, uma alta cobertura vacinal foi alcançada. Nenhum evento adverso grave foi notificado
FORMA FARMACÊUTICA
Shanchol é suspensão para administração oral.
VALIDADE
A data de validade da vacina é indicada no rótulo e na embalagem.
PRECAUÇÕES ESPECIAIS DE CONSERVAÇÃO
O Shanchol deve ser armazenado a temperaturas entre + 2ºC e + 8ºC. Não congele. Descarte se a vacina foi congelada.
APRESENTAÇÃO
Frascos de vidro contendo 1,5 mL em dose única.
INSTRUÇÃO DE UTILIZAÇÃO / MANUSEAMENTO
A vacina é apresentada como uma suspensão. Após agitação vigorosa do frasco, 1,5 mL deve ser derramado na boca do individuo. A administração da vacina pode ser opcionalmente seguida por água para facilitar a ingestão, se necessário. A vacina pode alternativamente ser administrada, em indivíduos mais jovens, utilizando uma seringa descartável (sem agulha) para retirar o conteúdo do frasco, que é então esguichado para a boca da criança. Shanchol não deve ser administrado por via parenteral (intramuscular / subcutânea ou intravenosa). A vacina é recomendada apenas para administração oral.
Instrução para Abrir Selo de Alumínio:

Fabricado por
Shantha Biotechnics Private Limited, India.
Referências:
Tradução e resumo do Prospecto Farmacológico do Shanchol – Shantha Biotechnics Private Limited. India.
Referências citadas no prospecto farmacológico do produto:
- PLoS ONE 2008; 3 (6): e2323.
- Lancet2009; 374: 1694-1702.
- PLoSNegl Trop Dis. 2011; 5 (10): e1
- Lancet Infectious Diseases 2013; 13 (12): 1050-1056.
- Clinical Infectious Diseases 2013; 56 (8): 1123-31.
- Vacina 2011; 29: 8285-8292.
- Vacina 2009; 27: 6887-6893.
- Dados em arquivo. Shantha Biotechnics Private Limited.
- Am J. Trop. Med. Hyg., 89 (4), 2013, pp. 671-681.
- 10 Am. J. Trop. Med. Hyg., 89 (4), 2013, pp. 617-624.
- PLoS Med 2013; 10 (9): e1001512. 12. PLoS Negl Trop Dis 2012; 7 (10): e2465.
CARACTERÍSTICAS DO DUKORAL – VACINA CONTRA A CÓLERA
NOME DO MEDICAMENTO
Dukoral suspensão e granulado efervescente para suspensão oral
Vacina contra a cólera (oral, inativada)
COMPOSIÇÃO QUALITATIVA E QUANTITATIVA
Cada dose de suspensão da vacina (3 ml) contém:
− Um total de 1,25×1011 bactérias das seguintes estirpes inactivadas:
Vibrio cholerae O1 Inaba, biotipo clássico e biotipo El Tor, e Vibrio cholerae O1 Ogawa, biotipo clássico,
− Subunidade B da toxina da cólera recombinante (rCTB) 1 mg (produzida em V. cholerae O1 Inaba, biotipo clássico estirpe 213.)
Excipientes:
2,0 mg de fosfato monossódico di-hidratado, 9,4 mg de fosfato de sódio dibásico di-hidratado, 26 mg de cloreto de sódio, 3600 mg de bicarbonato de sódio, 400 mg de carbonato de sódio anidro, 30 mg de sacarina sódica, 6 mg de citrato de sódio. Uma dose contém aproximadamente 1,1 g de sódio. Outros excipientes.
FORMA FARMACÊUTICA
Suspensão e granulado efervescente para suspensão oral.
A suspensão, acondicionada num frasco, é esbranquiçada. O granulado efervescente, acondicionado numa saqueta, é branco.
INFORMAÇÕES CLÍNICAS
Indicações terapêuticas
Dukoral é indicado para a imunização activa contra a doença provocada pelo Vibrio cholerae serogrupo O1 em adultos e crianças a partir dos 2 anos de idade que visitam áreas endémicas/ epidémicas.
Dukoral não deve substituir as medidas protetoras padrão. No caso de diarreia, devem ser instituídas medidas de reidratação.
Posologia e modo de administração
Posologia
Programa de vacinação primária
O curso primário padrão da vacinação com Dukoral contra a cólera é constituído por 2 doses para o adulto e criança a partir dos 6 anos de idade. As crianças entre os 2 e os 6 anos de idade devem receber 3 doses. As doses devem ser administradas a intervalos mínimos de uma semana. Caso decorram mais de 6 semanas entre as doses, o curso de imunização primária deve ser reiniciado. A imunização deve ser concluída pelo menos 1 semana antes da possível exposição a V. cholerae O1.

Dose de reforço
Para uma proteção mantida contra a cólera, recomenda-se uma dose única de reforço em 2 anos para o adulto e criança a partir dos 6 anos de idade, e no prazo de 6 meses para a criança entre os 2 e 6 anos de idade. Os dados imunológicos e sobre a duração da proteção sugerem que se tiverem decorrido menos de 2 anos depois da última vacinação para adultos e até 6 meses para crianças entre os 2 e os 6 anos se deve administrar uma dose de reforço. Se tiverem decorrido mais de 2 anos desde a última vacinação (mais de 6 meses para crianças entre os 2 e os 6 anos), o curso primário deve ser repetido.
Crianças com menos de 2 anos de idade
Em ensaios de segurança e imunogenicidade, procedeu-se à administração de Dukoral em crianças entre 1 e 2 anos de idade, mas a sua eficácia protetora não se encontra estudada neste grupo etário. Por conseguinte, a utilização de Dukoral não é recomendada em crianças com menos de 2 anos de idade.
Idosos
Apenas existem dados muito limitados sobre a eficácia protetora da vacina em indivíduos com 65 ou mais anos de idade.
Modo de administração
A vacina é administrada por via oral. Antes da ingestão, a suspensão deve ser misturada com uma solução tampão (bicarbonato de sódio). O bicarbonato de sódio é fornecido sob a forma de granulado efervescente que deve ser dissolvido num copo de água fria (aproximadamente 150 ml). Pode ser utilizada água clorada. A suspensão da vacina deve ser depois misturada com a solução tampão e bebida no prazo de 2 horas. Deve evitar-se a ingestão de sólidos e líquidos 1 hora antes e 1 hora depois da vacinação. A administração oral de outros fármacos deve ser evitada durante 1 hora antes e 1 hora depois da administração de Dukoral.
Crianças entre os 2 e os 6 anos de idade: metade da solução tampão deve ser rejeitada, e a parte restante (aproximadamente 75 ml) é misturada com a totalidade do conteúdo do frasco da vacina.
Contraindicações
Hipersensibilidade às substâncias activas, a qualquer um dos excipientes mencionados ou ao formaldeído.
A administração de Dukoral deve ser adiada em indivíduos apresentando doença gastrointestinal aguda ou doença febril aguda.
Advertências e precauções especiais de utilização
Dukoral confere proteção específica contra o Vibrio cholerae do serogrupo O1. A imunização não protege contra V. cholerae do serogrupo O139 nem contra outras espécies de Vibrio.
Em indivíduos infectados pelo VIH, os dados disponíveis relativamente à imunogenicidade e segurança da vacina são limitados. A eficácia protetora da vacina não se encontra estudada. A imunização de indivíduos infetados pelo VIH pode induzir aumentos transitórios da carga viral. Dukoral pode não induzir níveis protetores de anticorpos em indivíduos com doença avançada pelo VIH. No entanto, um estudo de eficácia, realizado numa população com elevada prevalência de VIH, revelou uma proteção similar à observada noutras populações.
A vacina não confere uma proteção completa, sendo importante cumprir adicionalmente medidas protetoras padrão para evitar a cólera.
Interações medicamentosas e outras formas de interação
A vacina é lábil aos ácidos. A ingestão de líquidos e/ou sólidos aumenta a produção de ácido no estômago e pode reduzir os efeitos da vacina. Por conseguinte, deve evitar-se a ingestão de sólidos e líquidos 1 hora antes e 1 hora depois da administração de Dukoral.
Deve evitar-se a administração de outras vacinas e medicamentos por via oral 1 hora antes e 1 hora depois da vacinação.
Fertilidade, gravidez e aleitamento
Não existem dados disponíveis de estudos em animais no que respeita à toxicidade reprodutiva. Depois de uma cuidadosa análise da relação benefícios/riscos, a vacina pode ser administrada durante a gravidez e amamentação, embora não se tenha efetuado qualquer ensaio clínico específico para avaliar este aspecto.
Efeitos indesejáveis
Reações adversas nos ensaios clínicos
A segurança de Dukoral foi avaliada em ensaios clínicos, incluindo adultos e crianças a partir dos 2 anos de idade e efectuados em países endémicos e não endémicos para a cólera e Escherichia coli enterotoxigénica (ETEC) produtora de enterotoxina lábil ao calor (LT).
Durante os ensaios clínicos foram administradas mais de 94.000 doses de Dukoral. As reações adversas notificadas com maior frequência, tais como sintomas gastrointestinais incluindo dor abdominal, diarreia, perda de consistência das fezes, náusea e vómitos, ocorrem com frequências semelhantes nos grupos de vacina e placebo.
Classificação de frequência: muito frequentes (≥1/10); frequentes (≥1/100, <1/10); pouco frequentes (≥1/1.000, <1/100); raros (≥1/10.000, <1/1.000); muito raros (<1/10.000), desconhecido (não pode ser calculado a partir dos dados disponíveis).
Os efeitos indesejáveis são apresentados por ordem decrescente de gravidade dentro de cada classe de frequência.
Doenças do metabolismo e da nutrição – Raros: Perda / diminuição do apetite; Muito raros: Desidratação.
Doenças do sistema nervoso – Pouco frequente: Cefaleias; Raros: Tonturas; Muito raros: Sonolência, insónias, desmaios, redução do paladar.
Doenças respiratórias, torácicas e do mediastino – Raros: Sintomas respiratórios (incluindo rinite e tosse).
Doenças gastrointestinais – Pouco frequentes: Diarreia, cólicas abdominais, dor abdominal, aumento dos ruídos gástricos/ abdominais (gases), desconforto abdominal; Raros: Vómitos, náuseas; Muito raros: Odinofagia, dispepsia.
Afeções dos tecidos cutâneos e subcutâneos – Muito raros: Sudação, exantema.
Afeções musculosqueléticas e dos tecidos conjuntivos – Muito raros: Dores articulares
Perturbações gerais e alterações no local de administração – Raros: Febre, mal-estar geral; Muito raros: Fadiga, calafrios.
Reações adversas na vigilância pós-comercialização
Em baixo, enumeram-se as reações adversas adicionais, notificadas durante a vigilância pós comercialização.
- Infeções e infestações: Gastroenterite
- Doenças do sangue e do sistema linfático: Linfadenite
- Doenças do sistema nervoso: Parestesias
- Vasculopatias: Hipertensão arterial
- Doenças respiratórias, torácicas e do mediastino: Dispneia, aumento da expetoração
- Doenças gastrointestinais: Flatulência
- Afeções dos tecidos cutâneos e subcutâneos: Urticária, angioedema, prurido
- Perturbações gerais e alterações no local de administração: Dor, síndrome gripal, astenia, calafrios
Sobredosagem
Os dados referentes à sobredosagem são limitados. As reações adversas notificadas são consistentes com as observadas depois da administração recomendada.
PROPRIEDADES FARMACOLÓGICAS
Propriedades farmacodinâmicas
Grupo fármaco terapêutico: Vacinas bacterianas, código ATC:J07AE01
Mecanismo de ação
A vacina contém bactérias V. cholerae O1 totais mortas e a subunidade B recombinante não tóxica da toxina da cólera (CTB). Estão incluídas na vacina estirpes bacterianas dos serotipos Inaba e Ogawa e dos biótipos El Tor e Clássico. Dukoral é administrado por via oral com tampão de bicarbonato, que protege os antigénios contra o ácido gástrico. A vacina actua induzindo a formação de anticorpos contra os componentes bacterianos e CTB. Os anticorpos antibacterianos intestinais impedem que a bactéria se fixe à parede intestinal, impedindo consequentemente a colonização de V. cholerae O1. Os anticorpos intestinais antitoxina impedem que a toxina da cólera se fixe à superfície da mucosa intestinal, prevenindo consequentemente os sintomas diarreicos mediados pela toxina.
A toxina lábil ao calor (LT) da E. coli enterotoxigénica (ETEC) é estrutural, funcional e imunologicamente semelhante a CTB. As duas toxinas apresentam uma reação cruzada do ponto de vista imunológico.
Eficácia contra a cólera
Eficácia de proteção contra cólera foi avaliada durante duas campanhas de vacinação em massa, realizadas em Moçambique (dezembro de 2003 – janeiro de 2004) e em Zanzibar (fevereiro de 2009 – maio de 2010). No estudo de controlo do caso, realizado durante a campanha de vacinação em massa em Moçambique, a eficácia de proteção de 2 doses de Dukoral foi 84% (IC a 95%: 43, 95; análise por protocolo; p = 0,005) para os 5 meses iniciais do seguimento.
PRECAUÇÕES ESPECIAIS DE CONSERVAÇÃO
Conservar no frigorífico (2ºC – 8ºC).
Não congelar.
Este medicamento mantém-se estável a temperaturas até 25°C durante um período de 14 dias, se conservado na embalagem exterior, com frasco e saqueta selados. No fim deste período, o medicamento deve ser utilizado ou eliminado.
Referência:
Tradução e resumo do artigo: European Medicines Agency/ Science Medicines Health; Relatório Público Europeu de Avaliação (EPAR) relativo ao Dukoral, 2014. https://www.ema.europa.eu/en/documents/product-information/dukoral-epar-product-information_en.pdf
RISCOS E BENEFÍCIOS DA VACINAÇÃO CONTRA CÓLERA NAS MULHERES GRÁVIDAS
O documento de posicionamento da OMS de 2010 sobre as vacinas contra a cólera, menciona especificamente as mulheres grávidas como um grupo que é “especialmente vulnerável a doenças graves e para as quais as vacinas não são contra-indicadas” e, portanto, um possível alvo para a vacinação.
A documentação actual dos produtores de VOCs pré-qualificados da OMS sobre seu uso durante a gravidez indica o seguinte:
Documentação Dukoral®
O folheto informativo da Dukoral® afirma que “A vacina pode ser administrada durante a gravidez e para mulheres lactantes.” No entanto, a monografia do produto Dukoral® afirma o seguinte: “O efeito do Dukoral® no desenvolvimento embrio-fetal não foi avaliado e não foram realizados estudos sobre toxicidade reprodutiva em animais. Não há estudos clínicos específicos realizados em função de este tema. A vacina não é, portanto, recomendada para uso na gravidez. No entanto, Dukoral® é uma vacina inativada que não se replica. Dukoral® também é administrado por via oral e actua localmente no intestino. Neste sentido, em teoria, Dukoral® não deve representar nenhum risco para o feto humano. A administração de Dukoral® a mulheres grávidas pode ser considerada após avaliação cuidadosa dos benefícios e riscos. ”
Instruções do folheto informativo Shanchol ™
“Não foram realizados estudos clínicos específicos para avaliar a segurança e imunogenicidade do Shanchol ™ em mulheres grávidas e para o feto. A vacina não é, portanto, recomendada para uso na gravidez. No entanto Shanchol ™ é uma vacina morta que não se replica, é administrada por via oral e actua localmente no intestino. Portanto, em teoria, Shanchol ™ não deve representar nenhum risco para o feto humano. A administração de Shanchol ™ a mulheres grávidas pode ser considerada após avaliação cuidadosa dos benefícios e riscos em caso de emergência médica ou epidemia ”.
Instruções do folheto informativo do pacote Euvichol®
“Não foram realizados estudos clínicos específicos para avaliar a eficácia e segurança do Euvichol em mulheres grávidas e no período de amamentação. Portanto, a vacina não é recomendada para uso na gravidez ”.
Esclarecimento da documentação dos produtores
Os documentos dos produtores não afirmam que a vacina é contraindicada durante a gravidez. A frase “a vacina é… não recomendado para uso na gravidez ”refere-se ao fato de que uma recomendação específica para seu uso durante a gravidez não foi feita devido à falta de dados sobre o uso da vacina em mulheres grávidas. Assim, nenhuma destas 3 vacinas é contra-indicada em mulheres grávidas.
O risco associado à cólera em mulheres grávidas
As taxas de perda fetal entre mulheres grávidas com cólera que estão em seu segundo ou terceiro trimestre variaram em estudos de 8% a 33%, enquanto as taxas de natimortos sozinhas (perdas no terceiro trimestre) entre essas mulheres em recentes estudos no Haiti e no Senegal foram encontrados 5,5 vezes e 1,8 vezes mais do que as taxas estimadas de natimortos nacionais, respectivamente.
Dois dos estudos, do Haiti e Bangladesh, também mostraram que a desidratação grave em mulheres grávidas com cólera aumenta significativamente o risco de natimortos ou abortos espontâneos – até nove vezes no estudo no Haiti. Além disso, uma parcela substancial de mulheres grávidas com cólera – 48% no Haiti – perdeu seus fetos antes de chegar ao hospital. Isto é provavelmente devido ao atraso na procura de cuidados de saúde entre as mulheres grávidas e ao facto de os fetos terem aparecido a morrer cedo no decurso da doença.
Estimar o grau de desidratação em mulheres grávidas é difícil, especialmente no final da gravidez, devido ao aumento normal no volume do plasma da mãe. Como resultado, os médicos podem subestimar o grau de desidratação. O tratamento da cólera em mulheres grávidas é, portanto, mais desafiador do que em outros pacientes e requer reposição de líquidos mais precoce e intensiva, bem como monitoramento rigoroso da reidratação.
Em conclusão, a cólera é mais grave em mulheres grávidas devido ao aumento do risco de complicações fetais e parto prematuro, associado a atrasos na busca de cuidados e dificuldades no manejo do paciente.
O risco associado à vacinação de mulheres grávidas com VOCs mortas
Nenhum ensaio clínico controlado de VOCs pré-qualificados pela OMS incluiu mulheres grávidas. No entanto, os dados disponíveis de dois inquéritos retrospectivos de mulheres vacinadas com VOC durante a gravidez – conduzidas na Guiné em 2012 e em Zanzibar em 2010 – não revelam qualquer aumento significativo nos resultados adversos maternos ou da gravidez em mulheres vacinadas em comparação com mulheres grávidas não vacinadas. Os dados de vigilância pós-comercialização do Dukoral®, bem como os dados de vigilância realizados durante o ensaio de eficácia do Shanchol ™, também não indicaram quaisquer efeitos adversos elevados em mulheres grávidas, embora tenha havido relativamente poucos relatos da sua utilização durante a gravidez.
Considerações semelhantes podem ser feitas para o perfil de segurança do Euvichol®, que tem a mesma formulação do Shanchol ™. Até hoje, não há evidências de que as vacinas mortas em geral sejam prejudiciais para as mulheres grávidas, seus fetos ou recém-nascidos e a maioria não é contra-indicada durante a gravidez. De fato, dois – vacinas contra influenza e toxóide tetânico – são especificamente recomendadas para todas as mulheres grávidas pela OMS e pelo CDC dos EUA, enquanto o CDC também recomenda a vacinação contra coqueluche durante a gravidez. O facto de a VOC ser administrada por via oral deve, em teoria, torná-la ainda mais segura do que as vacinas injetáveis mortas.
Potenciais benefícios da vacinação de mulheres grávidas com VOCs
O Shanchol ™ demonstrou proporcionar 74% de proteção a adultos (com 15 anos ou mais) durante um período de cinco anos. Embora existam poucos dados sobre a eficácia de VOCs mortos em mulheres grávidas, um estudo de coorte retrospectivo na Guiné após a vacinação em massa com Shanchol® mostrou que, entre as mulheres que engravidaram após as campanhas de vacinação, a incidência de cólera foi significativamente menor nas mulheres vacinadas durante as campanhas do que naquelas que não o fizeram. O ensaio randomizado e de não-inferioridade comparando Euvichol® e Shanchol ™ realizado nas Filipinas mostrou que um esquema de duas doses com Euvichol® induz uma forte resposta vibriocida comparável àquela provocada por Shanchol ™.
Além da provável redução das perdas fetais pela prevenção da cólera durante a gravidez, a vacinação de mulheres antes, durante ou logo após a gravidez pode reduzir o risco de cólera em seus bebês ou crianças pequenas. Isto deve-se ao papel importante das mães na transmissão da doença aos seus filhos e aos efeitos da vacinação de adultos na redução do risco de cólera em crianças demasiado jovens para receber a vacina. Numa reanálise de dados do ensaio clínico de vacinas orais mortas de cólera em Bangladesh, nas quais apenas foram vacinadas mulheres e crianças com dois anos ou mais, o risco de cólera em crianças não vacinadas com menos de dois anos de idade vivendo em áreas com alta cobertura de vacinação foi menos da metade da taxa entre crianças menores de dois anos vivendo em áreas com baixa cobertura vacinal.
Conclusão
VOCs só estão sendo fornecidos para populações consideradas de alto risco de cólera. Nessas situações, com base na análise dos riscos e benefícios, o GTFCC (WHO/ Global Task Force on Cholera Control) considera que há benefícios consideráveis e muito poucos riscos de incluir mulheres grávidas em uma campanha de vacinação. O GTFCC continuará a monitorar informações sobre a segurança da VOC durante a gravidez.
Referência:
Tradução e resumo do artigo publicado em:
Malária: Diagnóstico e Tratamento
A malária é uma doença infecciosa causada por um parasita unicelular (protozoário) do género Plasmodium (P). A doença é transmitida de uma pessoa para outra através da picada de mosquitos do género Anopheles (An.). Existem quatro espécies de Plasmodium que transmitem malária em humanos: P. falciparum, P. vivax, P. ovale e P. malariae. As duas primeiras espécies causam a maior parte dos casos de malária humana. O P. falciparum é responsável pela maior parte de casos graves e mortalidade por malária.
Para o efeito das normas do MISAU, a malária é classificada em termos clínicos em malária não complicada e malária complicada.
Diagnóstico
O diagnóstico da malária deve ser feito em qualquer doente que apresente uma síndrome febril aguda (suspeita) com um resultado positivo no teste de diagnóstico rápido (TDR), ou presença de Plasmodium no esfregaço de sangue.
Testes de Diagnóstico Rápido (TDR)
No País, devido à elevada prevalência do Plasmodium falciparum, são os mais indicados os testes do tipo “Histidine-richprotein 2 (HRP2)”. O teste de diagnóstico rápido pode permanecer positivo até 4 semanas após o diagnóstico inicial pelo que não deve ser usado para o seguimento do tratamento da malária.
Microscopia
Considerando que o maior volume de doentes será diagnosticado com base no TDR, recomenda-se que o resultado da microscopia seja expresso na forma de densidade parasitária (aplicável apenas para P. falciparum) em todos os doentes com pedidos de microscopia da malária.
Tabela 1: Definição de Hiperparasitemia (Malária Grave laboratorial)
| Classificação | Hiperparasitemia | |
| (DP)
|
Parasitas por
microlitro (p/μl) |
Percentagem de globulos
Vermelhos parasitados |
| Malária Grave | ≥100.000p/μl | GVp ≥2% |
MALÁRIA NÃO COMPLICADA
Definição: Malária sintomática sem sinais de gravidade ou evidência (clínica ou laboratorial) de disfunção de órgão vital. Os sinais e sintomas de uma malária não complicada são inespecíficos e estão resumidos no quadro abaixo indicado.
Quadro clínico da Malária não complicada

A FEBRE, a CEFALÉIA e as MIALGIAS são os sintomas mais frequentes da malária não complicada em zonas de alta transmissão como é o caso de Moçambique.
Tratamento da Malária Não Complicada
- Arteméter-Lumefantrina (AL): tratamento de eleição para o tratamento da malaria não complicada;
- Artesunato-Amodiaquina (ASAQ): tratamento alternativo para o tratamento da malaria não complicada (casos de alergia e/ ou contraindicação do medicamento de eleição, ou na falta deste);
- Quinino oral (primeiro trimestre da gravidez);
Deve-se evitar tratar as Síndromes Febris suspeitas de malária com antimaláricos sem confirmação laboratorial. O tratamento antimalárico deve ser dispensado apenas aos doentes com resultados positivos (TDR) e/ou quando se observam parasitas no sangue ou, excepcionalmente nos casos de suspeita em que não é possível confirmar a doença por falta dos meios auxiliares de diagnóstico (Malária clínica).
ARTEMÉTER-LUMEFANTRINA (AL):
Apresentação:
Comprimidos contendo 20 mg de Arteméter e 120 mg de Lumefantrina
Posologia:
O tratamento com Arteméter-Lumefantrina tem a duração de 3 dias e deve ser administrado de acordo com o peso ou idade do doente (ver tabela 2). O tratamento deve ser administrado de 12 em 12 horas (duas vezes por dia) durante 3 dias seguidos. É importante que o doente complete os 3 dias (6 tomas) de tratamento.
Tabela 2: Dose de Arteméter – Lumefantrina a ser administrada em 3 dias

Contra-indicações:
- Primeiro trimestre da gravidez;
- História de alergia aos derivados da Artemisinina (Artesunato, Arteméter) ou à Lumefantrina.
Em presença de qualquer destas situações, deve-se passar para o Quinino oral, Artesunato –Amodiaquina de acordo com a situação de cada doente.
ARTESUNATO (AS) + AMODIAQUINA (AQ):
Apresentação:
Comprimidos contendo 25 mg/67.5 mg (crianças), 50 mg/135 mg (adolescentes) e 100 mg/270 mg (adultos) de Artesunato e Amodiaquina base, respectivamente.
Posologia:
As doses da co-administração de AS + AQ são de 4 mg/kg e 10 mg/kg de peso/dia respectivamente, durante 3 dias (Tabela 3).
Tabela 3: Esquema de tratamento com Artesunato-Amodiaquina (combinação a dose fixa)

Contra-indicações: Artesunato+Amodiaquina (ASAQ):
- Hipersensibilidade conhecida a derivados de Artemisinina (Artesunato, Arteméter) ou a Amodiaquina;
- Primeiro trimestre da gravidez;
- Alterações hepáticas;
- Neutropenia;
- Retinopatia;
QUININO ORAL: QNN
Indicação:
Para o tratamento da Malária Não Complicada no 1º Trimestre da Gravidez ou em casos de contra indicação de outros medicamentos da malária não complicada.
Apresentação:
Comprimidos de 300 mg sulfato de quinino.
Posologia: Dose de 10 mg/kg de 8 em 8 horas, durante 7 dias.
Para todos os outros casos, a Tabela a seguir apresenta as doses a serem administradas de acordo com o peso e a idade (Tabela 4).
Tabela 4: Dose de Quinino a ser administrada por via oral*

* Os comprimidos devem ser tomados com água potável. Se ocorrer vómito na primeira meia hora após a administração do medicamento, deve repetir-se a toma. Se os vómitos persistirem deve ser colocada a hipótese de malária complicada.
MALÁRIA GRAVE /COMPLICADA
Definição: Num doente com parasitémia (formas assexuadas) por P. falciparum e sem outra causa óbvia para os sintomas, a presença de um ou mais dos seguintes achados clínicos ou laboratoriais, classifica o doente como sofrendo da malária complicada/grave.
Tabela 5: Manifestação Clínica da Malária Grave
| Manifestações Clínicas |
| § Prostração (fraqueza generalizada que impede o doente de andar e sentar);
§ Alteração da consciência coma (Glasgow <11 em adultos e Blantyre<3 em crianças); § Incapacidade de se alimentar; § Respiração profunda, dificuldade respiratória (respiração acidótica); § Convulsões repetidas (mais de dois episódios em 24h); § Colapso circulatório ou choque (TA sistólica <a 80mmHg nos adultos e <a 70mmHg nas crianças) segundo a OMS); § Edema pulmonar (radiológico) ou saturação do oxigénio <92%, frequência respiratória de>30 ciclos por minuto e crepitações na auscultação); § Hemorragia espontânea anormal; § Icterícia clínica e evidência de disfunção de outro órgão vital; § Hemoglobinúria (urina escura); § Anemia grave (palidez das mucosas e planta das mãos); § Hiperpirexia (temperatura axilar ≥ 39.5˚C); § Insuficiência renal (redução da diurese, urina cor de cocacola); |
| Achados Laboratoriais |
| § Hiperparasitémia: GVp ≥ 2% ou DP=100.000p/µl
§ Anemia normocítica grave Hb≤5g/dl ou hematócrito ≤15% em crianças <12 anos (<7g/dl e <20% respectivamente em adultos); § Hemoglobinúria; § Hipoglicémia (glicémia <2.2 mmol/l ou 40 mg/dl); § Acidose metabólica (bicarbonato plasmático <15 mmol/l); § Hiperlactatémia (lactato>5mmol/l); § Insuficiência renal (creatinina sérica>265µmol/l ou ureia >20 mmol/l); § Bilirrubina Plasmática>50µmol/(3mg/dl); |
Tratamento da Malária Grave/Complicada
- Artesunato injectável (EV, IM): tratamento de eleição
- Quinino injectável (EV, IM): tratamento alternativo

ARTESUNATO INJECTÁVEL:
Indicação:
Para o tratamento de todos os casos graves, incluindo mulheres grávidas em todos os trimestres e crianças menores de 5Kg de peso.
Apresentação:
Ampolas contendo 60 mg ácido artesúnico anídrico (pó) e uma ampola separada contendo solução de bicarbonato de sódio. As formas mais recentes podem apresentar uma terceira ampola contendo cloreto de sódio a 0,9% (soro fisiológico).
Preparação:
Dissolver o pó de Artesunato 60mg com todo conteúdo (1ml) de Bicarbonato de sódio 5% (que vem no pacote). Agite por 2-3min até dissolver.
A solução de Artesunato ficará inicialmente turva e depois deve ficar transparente (após agitação)
- Para via Endovenosa (EV): adicionar 5ml de NaCl 0,9% OU Dextrose 5%
- Para via Intramuscular (IM): adicionar 2ml de NaCl 0,9% OU Dextrose 5%
Atenção: A solução deve ser preparada para administração dentro de máximo de 1 hora e não pode ser armazenada para uso posterior.
Posologia:
- Em crianças com peso menor que 20Kg multiplicar Artesunato 3,0mg/kg pelo peso corporal para obter a quantidade de Artesunato (em mg) a ser administrada por cada dose.
1.a Em crianças com peso igual ou maior de 20Kg e adultos multiplicar 2,4 mg/kg pelo peso corporal para obter a quantidade de Artesunato (em mg) a ser administrada por cada dose.
- Para via Endovenosa (EV): dividir o resultado do passo 1 ou 1.a) por 10 para obter a dose em ml;
- Para a via Intramuscular (IM): dividir o resultado do passo 1 ou 1.a) por 20 para obter a dose em ml (administrar na porção anterior da coxa);
Administrar o Artesunato parenteral na quantidade obtida nos números 2 e 3 na hora 0 (admissão) seguida de 12/12 horas até completar 3 doses no 1º dia. Uma dose diária é indicada nos dias subsequentes até que o doente tolere a via oral (melhoria clínica e laboratorial) e passa para a dose completa do AL ou alternativo na dose completa (três dias). O Artesunato parenteral deve ser administrado no máximo de 7 dias.
Atenção: Logo que o doente tolere a medicação oral (pelo menos 24h após o tratamento injectável) passa para a administração oral do (Arteméter + Lumefantrina ou o alternativo) tratamento completo durante os 3 dias.
Contra-Indicações:
História de alergia aos derivados da Artemisinina (Artesunato, Arteméter)
QUININO INJECTÁVEL:
A administração rápida de quinino não é segura e nunca se deve dar directamente na veia pode levar a uma hipotensão letal.
Apresentação:
Ampolas de 300mg/ml de Dicloridrato de Quinino ou Ampolas de 600mg/2 ml de Dicloridrato de Quinino.
Posologia:
- Dose recomendada é de 10 mg/kg de Dicloridrato de Quinino pelo peso do doente e terá a quantidade em miligramas (mg) (para uma dose máxima de 600mg).
- Diluir o resultado do número 1 em dextrose a 5% na quantidade calculada em 10ml/kg pelo peso corporal do doente.
Administração:
Para via Endovenosa (EV): (gotas/min) durante 4 horas com intervalo de 8 em 8horas, logo que o doente tolere a via oral (mínimo 72h de medicação injectável) passar a medicação por via oral (ver tabela 4).
Atenção: Em doentes com insuficiência renal ou hepática, alterar o regime posológico para dar 10 mg/Kg de peso de 12 em 12 horas.
Contra-Indicações:
- Hipersensibilidade conhecida ao Quinino:
- Arritmias;
- Miastenia grave (risco de apneia);
Referência:
MISAU/Direcção Nacional de Saúde Pública/Programa Nacional de Controlo da Malária; Normas de Tratamento da Malária em Moçambique – 3ª. Edição. Maputo, Moçambique. 2017.
Dieta e exercícios reduzem o risco de diabetes em pessoas com HIV

27/03/2019
Autor: Roger Pebody – Editor of NAM’s website aidsmap.com and co-edits HIV & AIDS Treatment in Practice
As taxas de diabetes são mais altas em pessoas que vivem com o HIV do que na população geral, mas conselhos de estilo de vida individualizados de um nutricionista pode levar a reduções clinicamente e estatisticamente significativas da glicose, peso e outros factores de risco de acordo com um pequeno estudo realizado em Londres na área de Medicina Diabética.
Contextualização
“Existem barreiras significativas à mudança de hábitos alimentares e de estilo de vida dentro do HIV, incluindo estigma, isolamento e desafios da imagem corporal, que devem ser levados em consideração ao projectar intervenções de prevenção do diabetes”, comentou Alastair Duncan do Guy and St Thomas ‘Hospital . Seus métodos mistos fornecem dados qualitativos que dão uma visão sobre os factores que motivam os indivíduos a mudar seu estilo de vida ou que impedem a mudança de comportamento.
Estudos anteriores de intervenções no estilo de vida com pessoas com HIV focaram principalmente no risco cardiovascular e não tiveram impacto no risco de diabetes.
Objectivos
A intervenção teve como objectivo alcançar perda de peso moderada por meio da restrições de consumo de alimentos de alto conteúdo calórico e o aumento da actividade física, juntamente com reduções na gordura saturada, açúcar e sal, e aumento no consumo de cereais integrais, frutas e legumes.
Metodologia
A intervenção avaliada envolveu seis visitas mensais individuais, cada uma com duração de 30 minutos, em que um nutricionista forneceu aconselhamento individualizado sobre como fazer mudanças no estilo de vida.
Vinte e oito pessoas vivendo com HIV concluiram o processo de intervenção.
Foram utilizadas técnicas de entrevista motivacional e terapia cognitivo-comportamental, como estabelecimento de metas e autocontrolo. Os objectivos foram individualizados: por exemplo, o aconselhamento dietético foi adaptado à etnia, hábitos alimentares, status socioeconômico, padrões de estilo de vida, acesso a alimentos, capacidade de cozinhar e questões médicas.
Metas mensais para atingir meta desejada foram acordadas conjuntamente pelo nutricionista e pelo participante.
Como critério de inclusão, todos apresentavam níveis de glicose em jejum (6,0 – 6,9 mmol / l) indicando “pré-diabetes” – um risco aumentado de desenvolver diabetes. Um nível acima disso indicaria diabetes. Sua idade média era de 54 anos, três quartos eram homens e eram etnicamente diversos.
No início, o índice de massa corporal médio foi de 30,5 (níveis acima de 30 indicam obesidade), 57% tinham hipertensão, 79% síndrome metabólica, 61% esteatose hepática e 4% doença cardiovascular.
Os participantes estavam em tratamento para o HIV há uma média de dez anos e pouco menos da metade já havia tomado anti-retrovirais que podem contribuir para o risco de diabetes (zidovudina, estavudina, didanosina, indinavir, lopinavir).
Dos dez objectivos de estilo de vida propostos, os participantes alcançaram uma média de cinco metas. A meta mais frequentemente alcançada, reduzr a ingestão de sódio para <2,5 g por dia, foi atingida por 82% dos participantes, 61% alcançaram restrição de açúcar adicionado a <25g por dia, 57% alcançaram 10.000 passos por dia e 57% capaz de restringir a gordura saturada a <10% do consumo total de energia.
No entanto, apenas 22% foram capazes de atingir a meta de 7% de perda de peso e 14% alcançaram o objectivo de aumentar a ingestão de gordura monoinsaturada para> 15% da ingestão total de energia. No entanto, alguns desses objectivos foram parcialmente alcançados.
Comparando os resultados no início e no final da intervenção de seis meses, o programa reduziu significativamente:
- glicose em jejum (queda de 7,9%, de 6,3 para 5,8 mmol / l)
- área incremental de glicose sob a curva em um teste de tolerância a refeição (abaixo de 17,6%, de 255 a 210 mmol / l x min)
- insulina em jejum (queda de 22,7%, de 100,1 para 77,1 pmol / l)
- área incremental de insulina sob a curva em teste de tolerância a refeição (queda de 31,4%, de 1870 a 1283 pmol / l x min)
- peso (abaixo de 4,6%, de 88,8 a 84,7 kg)
- circunferência da cintura (abaixo de 6,2%, de 107,1 a 100,5cm)
- pressão arterial sistólica (queda de 7,4%, de 135 para 125 mmHg)
- triglicerídeos (queda de 36,7%, de 2,07 para 1,31 mmol / l)
Os pesquisadores observam que essas reduções são maiores do que as reduções tipicamente vistas em estudos do “mundo real” com participantes em grande parte soronegativos, como a glicemia de jejum reduzida em 0,09 mmol / l e o peso reduzido em 2,5kg. Em estudos populacionais gerais, essas alterações estão associadas a uma redução de 29% na incidência de diabetes.
Dados qualitativos
Entrevistas semi-estruturadas foram realizadas com 15 dos 28 participantes, e também com oito indivíduos que se recusaram a participar ou desistiram. Os participantes geralmente acharam a intervenção aceitável, particularmente apreciando melhor conhecimento e habilidades, entrevista motivacional, ajuste gradual de metas com ferramentas como pedômetros e apoio mensal.
Eles perceberam que a intervenção tem potencial para impactar uma ampla gama de preocupações com a saúde:
“Ele não apenas se livra da gordura da barriga, é bom para o coração e para o mental também” (homem de 60 anos).
Aqueles capazes de fazer mudanças de comportamento foram muitas vezes motivados por ter um senso de controle sobre a prevenção do diabetes. Eles tinham mais acesso ao apoio social do que aqueles que não alcançaram metas.
Aqueles que se recusaram a participar da intervenção descreveram as consultas mensais como onerosas. As entrevistas também identificaram algumas barreiras à mudança de comportamento que são específicas para o HIV. Em primeiro lugar, as alterações na forma corporal associadas à lipodistrofia afetaram a imagem corporal e o conforto de alguns participantes com o exercício:
“Meu estômago. Toda vez que vou ao ginásio, as pessoas pensam que estou grávida por causa da lipodistrofia ”(mulher de 55 anos).
Entrevistados de todas as etnias temiam que a perda de peso pudesse levar à revelação do HIV ou estar associada a doenças relacionadas ao HIV:
“Se eu perder peso… a primeira coisa que eles vão apontar, aquele tem SIDA. Por causa do peso que você perdeu”(mulher de 49 anos).
Participantes de origem africana descreveram excesso de peso como culturalmente desejável. Uma perda de identidade cultural pode ser uma barreira significativa para a redução de peso:
“Eu disse:” Oh, olhe o quão grande eu sou “. Eles disseram: “Ah, não, você não é grande, essa é a coisa certa”… Eles disseram: “não, não, não, não emagreça” (mulher de 51 anos).
Alguns entrevistados atribuíram seu risco aumentado aos medicamentos para o HIV e consideraram medidas de prevenção fúteis. Esses indivíduos tenderam a não alcançar os objetivos de intervenção ou a diminuir a participação na intervenção.
“Conforme você envelhece e está com essas drogas [HIV], isso [diabetes] vai acontecer. Não há nada que você possa fazer. Você pode tentar ser saudável, mas não vai evitá-lo ”(homem de 46 anos).
“Eu tenho um problema por causa da medicação para o HIV que estou tomando porque sei que me faz engordar” (homem de 40 anos).
Mas para os entrevistados que alcançaram mais metas, o desejo de evitar aumentar o peso da medicação ou a carga da doença motivou a mudança de comportamento.
“Ter que começar a tomar remédios contra diabetes também, além dos HIV, pensei, isso vai ser muito difícil” (mulher de 48 anos).
Alguns acreditavam que a prevenção do diabetes era viável e menos onerosa do que viver com o HIV:
“Diabetes é uma doença, mas sei que pode ser facilmente combatido com alimentos sem tomar nenhum remédio. Mas o HIV não é assim ”(homem de 71 anos).
Os pesquisadores concluem: “Nós demonstramos os efeitos benéficos de uma intervenção no estilo de vida em mitigar o aumento do risco de diabetes tipo 2 associado ao HIV. Intervenções futuras devem ser planejadas para reduzir ainda mais as barreiras únicas que impedem os resultados bem-sucedidos nessa coorte. ”
Referência
Duncan AD et al. Reducing risk of Type 2 diabetes in HIV: a mixed‐methods investigation of the STOP‐Diabetes diet and physical activity intervention. Diabetic Medicine, 7 February 2019. http://www.eatg.org/news/diet-and-exercise-advice-lowers-diabetes-risk-in-people-with-hiv/
Fumo de tabaco destrói corações

Todos os anos, o tabaco mata mais de 7 milhões de pessoas, o que significa que cada dia, 19.000 pessoas morrem em consequência do uso ou exposição ao fumo de tabaco. A maioria das mortes relacionadas ao tabaco é registada em países de baixa e média renda, onde a população está sujeita a táticas intensivas de marketing da indústria do tabaco.
Mas o tabaco também pode ser mortal para os não-fumadores: o fumo passivo produz doenças cardíacas, cancro e outras doenças, e é a causa de cerca de 890.000 mortes prematuras a cada ano. A magnitude do caos que o tabaco causa na saúde das pessoas é surpreendente. Mas essas mortes podem ser evitadas. A indústria do tabaco continua a incentivar vigorosamente o consumo do tabaco e fazer todo o possível para esconder os perigos seus produtos levam consigo, mas estamos firmes para combatê-los.
A nível mundial, um em cada três óbitos é consequência de doenças cardiovasculares (DCV), apesar da disponibilidade de tratamentos eficazes, econômicos e seguros. De fato, as DCVs são a principal causa mundial de morte, e eles retiram a vida a cerca de 18 milhões de pessoas cada ano, 80% destas pessoas em países de baixa e média renda como Moçambique.
O consumo de tabaco e a exposição ao fumo passivo estão entre as principais causas de DCV, e contribuem para aproximadamente 17% das mortes globais por DCV, ou seja, cerca de 3 milhões de mortes por ano.
O risco cardiovascular aumenta com a quantidade de tabaco fumado e os anos de consumo. No entanto, embora exista uma relação clara entre a quantidade de tabaco fumado por dia e risco cardiovascular, essa relação não é linear. O risco aumenta consideravelmente mesmo com baixa exposição ao fumo de tabaco, como ocorre com a exposição ao fumo alheio (fumador passivo). De facto, fumar apenas um cigarro por dia implica metade do risco de doença coronária e acidente vascular cerebral (AVC) do que fumar 20 cigarros por dia.
A exposição ao fumo passivo pode causar doença cardíaca coronária em adultos e aumenta o risco em torno de 25% a 30%. As DCV são, de longe, a principal causa de morte associada à exposição ao fumo passivo. Cerca de 55% das quase 890.000 mortes de adultos que ocorrem todos os anos no mundo devido à exposição ao fumo alheio são atribuíveis à cardiopatia isquémica.
No relatório de 2014 sobre tabaco, o Departamento de Saúde dos Estados Unidos da América concluiu que existe uma relação causal entre a exposição ao fumo passivo e eventos cardiovasculares agudos, e que a aplicação de leis e políticas sobre ambientes sem fumo de cigarro reduz significativamente esses episódios em não-fumadores com menos de 65 anos de idade.
O fumo do tabaco contém mais de 7000 substancias químicas e está composto por duas fases:
1. A fase de partículas e uma fase gasosa. O primeiro contém nicotina, uma substância muito viciante que aumenta a frequência cardíaca, pressão arterial e contratilidade do miocárdio e alcatrão de tabaco que, combinados, contribuem para as cardiopatias através dos seguintes mecanismos: inflamação, alteração do endotélio capilar, aumento da coagulabilidade e redução do colesterol de lipoproteínas de alta densidade.
2. A fase gás contém, entre outros, monóxido de carbono, um gás venenoso que substitui o oxigênio no sangue, reduzindo o oxigênio disponível para o músculo cardíaco e outros tecidos do organismo.
Esses efeitos fisiopatológicos do tabaco predispõem usuários ativos de tabaco e a fumadores passivos à aterosclerose (estreitamento das artérias), o que pode causar diferentes tipos de DCV, como cardiopatia isquémica, acidente vascular cerebral, arteriopatias periféricas e aneurismas válvulas aórticas. Todos os produtos do tabaco são intrinsecamente prejudiciais, incluindo aqueles que não produzem fumo, que contêm mais de 2.000 produtos químicos, incluindo a nicotina. Eles também contêm metais pesados, como o cádmio, e aditivos, como o alcaçuz ou as cinzas queimadas do fungo Phellinus igniarius (“cinza do punk”), que são prejudiciais ao sistema cardiovascular. Os produtos do tabaco sem fumo (tabaco mastigado, cigarros electrónicos) também podem causar doenças cardíacas porque elevam a pressão arterial de forma aguda e causam hipertensão crônica. Revisões de outros estudos mostraram que há uma relação entre o consumo de tabaco sem fumaça e morte por infarto do miocárdio e acidente vascular cerebral. O consumo deste tipo de produto está crescendo em muitas partes do mundo, e em alguns países, como Bangladesh ou Índia, é mais frequente do que o consumo de tabaco fumado.

Referência:
Organización Mundial de la Salud; El tabaco rompe corazones. Elija salud, no tabaco. Ginebra. 2018. (WHO/NMH/PND/18.4)
Cólera: Avaliação Clínica e Tratamento
A cólera é uma doença diarreica aguda causada pela enterotoxina do Vibrio cholerae, através da ingestão de alimentos ou água contaminados pela bactéria Vibrio cholerae. Tem um período de incubação curto, que varia de duas horas a cinco dias, e manifesta-se com diarreia aquosa e profusa, com ou sem vômitos, dor abdominal e cãibras, que quando não tratada prontamente, pode evoluir para a desidratação grave, acidose e colapso circulatório, com choque hipovolêmico e insuficiência renal e, consequentemente a morte em poucas horas.
Factos importantes:
- A cólera é uma doença diarreica aguda que pode matar em poucas horas se não for tratada.
- Até 80% dos casos podem ser tratados com sucesso com sais de re-hidratação oral.
- Medidas de controlo eficazes dependem da prevenção, preparação e resposta.
- Fornecimento de água potável, alimentos seguros e o saneamento básico são fundamentais para reduzir o impacto da cólera e outras doenças de transmissão oro-fecal e hídrica.
- Educação em saúde para a comunidade é importante para a adopção de comportamentos preventivos para evitar a contaminação.
- Fornecimento de água potável, saneamento básico e segurança alimentar são fundamentais para a prevenção da ocorrência de cólera.
- Existem vacinas orais, consideradas um meio adicional para controlar a cólera, mas que não substituem as medidas de prevenção e controlo convencionais.
Modo de transmissão
Uma vez que a transmissão da cólera está associada à gestão inadequada do meio ambiente, a falta de água potável, higiene individual e colectiva deficiente, a transmissão ocorre, principalmente, pela ingestão de água ou alimentos contaminados por fezes ou vómitos de um doente ou portador. A contaminação pessoa a pessoa é também importante na cadeia epidemiológica.
Manifestações clínicas:
A cólera manifesta-se de forma variada, desde infecções inaparentes até diarreia profusa e grave. Além da diarreia, podem surgir vômitos, dor abdominal e, nas formas severas, cãibras, desidratação e choque. A febre não é uma manifestação comum. Portanto, a doença pode manifestar-se de 2 formas:
- Na forma grave, os casos graves mais típicos (menos de 10% do total), o início é súbito, com diarreia aquosa, profusa, com inúmeras dejeções diárias, por vezes do tipo “água de arroz” e cheiro a peixe, com ou sem vómitos, dor abdominal e cãibra. A diarreia e os vômitos, nesses casos, determinam uma extraordinária perda de líquidos, que pode ser da ordem de 1 a 2 litros por hora. Este quadro, quando não tratado de imediato, pode evoluir para desidratação rápida, acidose, colapso circulatório, com choque hipovolémico, insuficiência renal e morte, em 6 horas.
- A forma leve ou oligossintomática, apresenta-se com diarreia leve, como acontece na maioria dos casos.
Cerca de 80% das pessoas infectadas com o vibrião colérico são assintomáticas, embora a bactéria esteja presente nas suas fezes e sejam eliminadas de volta para o meio ambiente, podendo potencialmente infectar outras pessoas, ou a água e os alimentos.
Complicações:
As complicações na cólera decorrem, fundamentalmente, da depleção hidro-salina causada pela diarreia e pelos vômitos. Ocorrem mais frequentemente nos indivíduos idosos, diabéticos ou com patologia cardíaca prévia. A desidratação não corrigida levará a uma deterioração progressiva da circulação, da função renal e do balanço hidroeletrolítico, produzindo dano a todos os sistemas do organismo. Em consequência, sobrevém choque hipovolêmico, necrose tubular renal, íleo paralítico, hipocalemia (levando a arritmias), hipoglicemia (com convulsão e coma em crianças).
O aborto é comum no 3º trimestre de gestação, em casos de choque hipovolêmico. As complicações podem ser evitadas, com hidratação adequada.
Avaliação clínica do paciente
A observação dos sinais e dos sintomas é fundamental para que se possa classificar o paciente quanto ao seu estado de hidratação no decorrer da diarréia de qualquer etiologia, inclusive a causada pela cólera, com a finalidade de identificar o grau de desidratação e decidir sobre o plano de reposição.
Quadro 2: Avaliação do grau de desidratação do doente


A avaliação do estado de hidratação do paciente é baseada na presença dos sintomas e sinais apresentado no Quadro 3.
Quadro 3: Classificação do estado de hidratação

Tratamento
O tratamento dos casos de cólera e de outras diarreias agudas de acordo com as normas em vigor no País, implica:
- Determinar o grau de desidratação do doente (Quadro 2).
- Administrar líquidos, de acordo com o plano de tratamento.
- Recolher uma amostra de fezes dos 5 primeiros doentes com suspeita de cólera e de outras Diarreias Agudas que forem observados na unidade sanitária.
A rehidratação rápida e adequada é a principal intervenção para o tratamento de casos de cólera, quer por via oral para os casos moderados, ou por via intravenosa para casos graves. Até 80% dos pacientes podem ser tratados adequadamente por meio da administração de SRO. Os doentes graves e desidratados são tratados através da administração de fluidos intravenosos, de preferência Lactato de Ringer.
A administração de antibióticos adequados está indicada apenas para os casos graves para diminuir a duração da diarreia, reduzir o volume de fluidos para hidratação necessários e encurtar a duração da doença.
Para as crianças de 0 a 5 anos, a administração suplementar de zinco tem-se mostrado eficáz na redução da duração da diarreia, bem como redução de sucessivos episódios de diarreia. O suplemento deve ser iniciado no início dos sintomas. A Tabela 3 apresenta a dose de zinco a administrar às crianças com cólera.
Tabela 3: Dose de zinco a administrar durante o tratamento de crianças com cólera.

Rehidratação
Este é o componente essencial do tratamento, cujo objectivo é o de repor a água e electrólitos perdidos através da diarreia e vómitos. Nas Tabelas 5, 6 e 7 é apresentada a rehidratação segundo os planos de tratamento A, B, C.
Note que, a reposição de líquidos por via oral é a preferida, enquanto a reposição intravenosa é reservada para a rehidratação de pacientes com desidratação grave ou que eliminam mais de 10-20 ml/kg/h. Administra-se por sonda nasogástrica.
Tabela 5: Rehidratação segundo o plano de tratamento A

Tabela 6: Rehidratação segundo o plano de tratamento B

Tabela 7: Rehidratação segundo o plano de tratamento C

Em relação ao Plano C:
- É extremamente importante manter um registo escrito de perda de fluido e consumo, a fim de ajustar a administração de fluidos para os pacientes.
- Se o doente vomitar enquanto toma SRO, esperar 10 minutos e depois continuar a darlhe líquidos mais lentamente.
- Continuar a amamentação dos bebés e crianças pequenas.
Tratamento com antibiótico
Além de rehidratação, é recomendado o tratamento antibiótico apenas nos casos com desidratação grave. A terapia antimicrobiana é útil para (a) rápida eliminação do vibrião, (b) diminuir a duração da diarreia, e (c) diminuir a perda de líquidos.
Tabela 9: Dosagem de antibióticos no tratamento de doentes gravemente desidratados com cólera

Referência:
MISAU/Direcção Nacional de Saúde Pública/Departamento de Epidemiologia; Manual de Prevenção e Controlo da Cólera e de Outras Diarreias Agudas – 4ª. Edição. Maputo, Moçambique. 2016.
Cancro do Colo do Útero, Câncer Cervical, ou Câncer do colo de útero
Cancro do colo do útero é um tipo de tumor maligno que ocorre na parte inferior do útero, no cervix. O câncer cervical é o terceiro câncer mais comumente diagnosticado em todo o mundo e a quarta principal causa de morte por câncer em mulheres. O câncer cervical causa cerca de 266.000 mortes em todo o mundo. A taxa de mortalidade é dez vezes maior nos países em desenvolvimento em comparação com os países desenvolvidos. Nas últimas décadas, a incidência de cancro do colo do útero diminuiu em um terço e a mortalidade em metade. Está comprovado que o programa de rastreamento do colo do útero está associado com o aumento da taxa de cura do cancro do colo do útero. Este tipo de cancro é mais comum em pessoas com idades entre 25 e 34 anos.
O cancro do colo do útero é uma das primeiras dez causas de morte de mulheres em Moçambique.

O Vírus HPV
O cancro do colo do útero é causado por uma infecção persistente pelo papilomavírus humano (HPV). O Vírus HPV transmite‐se principalmente pelo contacto sexual, ficando alojado na área genital dos homens e mulheres, mas existem outras vias como: o canal de parto, o uso de materiais contaminados (por exemplo: roupas íntimas, toalhas, etc…).

Dos 150-200 tipos de HPV conhecidos, os tipos 16 e 18 do vírus do papiloma humano (HPV) causam 75% dos cânceres do colo do útero em todo o mundo, enquanto os tipos 31 e 45 são a causa de mais 10% dos casos. Mulheres com múltiplos parceiros sexuais (ou que tenham relações sexuais com homens que têm ou tiveram muitos outros parceiros) estão em maior risco de desenvolver o câncer. Acredita-se que a infecção pelo HPV seja uma condição necessária para o desenvolvimento do câncer do colo do útero.
Factores de Risco
- Início precoce da vida sexual.
- Grande quantidade de parceiros sexuais, aumenta o risco de contrair HPV.
- Presença de outras DSTs, como gonorreia, sífilis, clamídia ou HIV.
- Sistema imunológico debilitado permite que o HPV tenha mais possibilidades de se manifestar.
- Tabagismo pode aumentar incidência de carcinoma de células escamosas.
- Uso prolongado de pílula anticoncepcional (por mais de 5 anos).
- Histórico de três ou mais gestações.
- Uso de DIU.
- Histórico familiar de câncer de colo do útero.
Sinais e Sintomas
As lesões ou feridas iniciais no colo do útero provocadas pelo vírus HPV podem não provocar sintomas. Quando a doença se agrava para cancro do colo do útero normalmente a mulher pode sentir ou ter:
- Sangramentos vaginais anormais, por exemplo hemorragias entre as menstruações, hemorragia durante ou após as relações sexuais, e hemorragias após a menopausa;
- Corrimento vaginal anormal, aumentado e que se repete, por vezes com mau cheiro;
- Dor durante as relações sexuais;
- Dor na pelve.
Os sintomas do cancro do colo do útero avançado incluem: perda do apetite, emagrecimento, fadiga, dor pélvica, dor lombar, dores e inchaço nas pernas, sangramento vaginal de grande volume, fraturas e, mais raramente, perda de urina e fezes pela vagina. Sangramento após ducha vaginal ou após o exame ginecológico é um sintoma comum do câncer do colo do útero.
Na consulta o técnico pode realizar perguntas que lhe permitam identificar melhor a presença de um provável cancro cervical, tais como:
- Quais são os seus sintomas? Apresenta sangramento vaginal irregular?
- Quando você começou a apresenta-los?
- Você faz os exames de Papanicolau desde que têm uma vida sexual activa? Já apresentou um resultado deste exame anormal?
- Você já foi tratada devido a algum problema no colo do útero?
- Você já foi diagnosticada com alguma ITS?
- Você fuma ou já fumou? Em que quantidades?
Uma mulher que tenha sido infectada pelo HPV desenvolve uma lesão (ferida) no colo do útero, que pode levar até 10 a 20 anos para desenvolver o cancro do colo do útero.

Diagnóstico
O cancro do colo do útero em estágio inicial pode ser rastreado pelo técnico nas consultas de rotina. Para detectá-lo ou as lesões do HPV os exames mais usados são:
- Papanicolau
- Colposcopia e vulvoscopia, com biópsia se necessário.
- Os exames de prevenção costumam ser feitos depois que a mulher começa a ter uma vida sexual activa.
Quando o câncer de colo do útero já está em curso, outros exames podem ser feitos para identificar a extensão do tumor:
- Biópsia da região
- Tomografia computadorizada
- Ultrassom
- Ressonância magnética
- Tomografia por emissão de pósitrons (PET-Scan).

Estadiamento
O cancro do colo do útero é estadiado a partir do sistema estabelecido pela Federação Internacional de Ginecologia e Obstetrícia (FIGO), que se baseia mais no exame clínico do que nos achados cirúrgicos. Apenas os testes e métodos não invasivos a seguir podem ser usados no estadiamento da doença, quando se utiliza o sistema FIGO: palpação, inspeção, colposcopia, curetagem endocervical, histeroscopia, cistoscopia, proctoscopia, urografia intravenosa, conização e radiografia do tórax e do esqueleto.
|
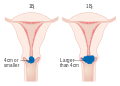
Estádio I: Tumor limitado ao colo |
|
|
Estádio 1a Carcinoma invasivo diagnosticado só por microscopia |
Estádio 1b Lesões invasivas clinicamente visíveis limitadas ao colo ou lesão visível no microsocopio >IA2 |
 |
 |
|
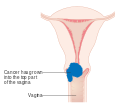
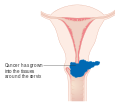
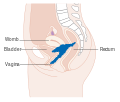
Estádio II: Tumor com invasão para além do útero sem atingir a parede pélvica ou o terço inferior da vagina |
|
| Estádio 2a
Sem invasão dos paramétrios |
Estádio 2b Com invasão dos paramétrios mas não da parede pélvica |
 |
 |
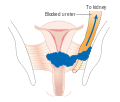
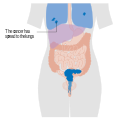
| Estádio III:
Extensão para a parede pélvica e/ou envolvimento do 1/3 inferior da vagina e/ou hidronefrose ou rim não funcionando |
|
| Estádio 3b
Extensão para a parede pélvica e/ou hidronefrose ou rim não funcionando |
|
 |
|
|
Estádio IV Extensão para além da pélvis ou envolvimento da mucosa da bexiga ou recto |
|
| Estádio 4ª
Tumor com invasão de órgãos adjacentes |
Estádio 4b Tumor com invasão de órgãos à distância |
 |
 |
Prevenção
O Cancro do Colo do Útero PODE SER PREVENIDO!
- Vacinar as meninas contra o HPV entre a idade de 9 e 20 anos. A vacina reduz o risco de desenvolver o câncer cervical em 93% e também protege contra o câncer de vagina, câncer de vulva, câncer retal, câncer de faringe e câncer de boca, que também associados ao HPV. A vacina nos homens também previne cânceres masculinos como o câncer de pênis e a transmissão do HPV para mulheres.
- Uso de preservativo em todas relações sexuais.
- Mudança de comportamentos sexuais de risco para reduzir a transmissão de doenças sexuais
- Adiamento das relações sexuais nas meninas,
- O rastreio e tratamento das lesões ou feridas iniciais do colo do útero. Através do exame de Papanicolaue da colposcopia é possível realizar a monitorização das mulheres saudáveis para detectar lesões intracervicais (CIL). O exame deve ser repetido a cada 5 anos em mulheres sem factores de risco, a cada 3 anos com baixo risco e anualmente quando há alto risc O primeiro exame normalmente é feito entre os 20 e os 30 anos.
No País, algumas unidades sanitárias já estão a fazer o rastreio do cancro do colo do útero e o tratamento imediato das lesões iniciais antes de estas se transformarem em lesões malignas. O técnico de saúde deve transferir as utentes com sinais e sintomas para uma unidade sanitária para o rastreio.
Tratamento
O tratamento geralmente é por cirurgia, radioterapia e quimioterapia, e depende das condições do paciente, do tipo de tumor e da sua procedência.
Prognóstico
A sobrevivência 5 anos após o diagnóstico é em média de 72%. Nos estágios iniciais é de 92%, caindo 35% nos estágio III e 15% no estágio IV. Cerca de 35% das mulheres com câncer invasivo voltam a ter esse câncer em menos de 5 anos. Geralmente as metástases são locais, invadindo vagina, bexiga, cólon, reto e peritônio.
Referências
- Louise Newson; Cervical Cancer https://patient.info/doctor/cervical-cancer-pro
- World Cancer Report 2014: World Health Organization. 2014. pp. Chapter 1.1. ISBN 9283204298
- Bosch, FX; de Sanjosé, S (2007). «The epidemiology of human papillomavirus infection and cervical cancer.». Disease Markers.
- Cervical Cancer Prevention (PDQ®). National Cancer Institute. 27 de fevereiro de 2014.
- Bermudez, Adriana e Col.; Câncer do colo do útero, FIGO CANCER REPORT 2015.
VISÃO GERAL DE TUBERCULOSE EM PROFISSIONAIS DE SAÚDE DE MOÇAMBIQUE
Autor: Maria Mico Polana
A tuberculose constitui um grave problema de saúde pública, com grande repercussão mundial. A sua presença, concomitante vem suscitando diversos impactos negativos na comunidade em geral.
Em Moçambique, a TB constitui uma das causas mais comuns de morbi-mortalidade em indivíduos vivendo com HIV/SIDA, tendo em conta que 36% de novos casos da tuberculose são co–infetados pelo HIV e, a taxa de óbito rondou em 6% em 2018. A importância clinica e epidemiológica da doença em nosso meio é amplamente conhecida pois, segundo a OMS, estima-se que cerca de 163 mil pessoas são infetadas anualmente pela doença em Moçambique.
Todavia este cenário, faz com que o controlo e prevenção da TB na comunidade e nos serviços de prestação de cuidados de saúde, represente um desafio a todos os níveis da esfera de saúde publica, o qual é aumentado pelo surgimento de cada vez mais de formas de TB Resistente (TBMR) implicando necessariamente maior esforço em termos de recursos humanos, financeiros e logísticos para o combate da epidemia.
Entre os grupos de risco para essa infecção estão os trabalhadores de saúde – um dos grupos de risco de contrair a doença, associado ao tempo de exposição a pacientes com a doença durante o serviço, a demora no diagnóstico bem como o incumprimento das medidas administrativas de controlo ambiental e de proteção respiratória individual. Como consequência, há um risco acrescido da probabilidade da ocorrência da transmissão nosocomial quando as medidas preventivas que visam salvaguardar a saúde do trabalhador são deficientes ou inexistentes.
O Ministério de Saúde de Moçambique, através do Programa Nacional de Controlo da Tuberculose implementa desde 2008, o programa de Controlo de Infecções por TB (CITB) nas unidades sanitárias do país e, neste âmbito em 2010 a Jhpiego, parceiro de cooperação do MISAU, apoiou na realização do primeiro estudo nacional intitulado “Avaliação rápida: Risco de transmissão da TB e grau de cumprimento das medidas de CITB nos locais de cuidados de saúde em Moçambique”. O citado estudo serviu de base para a definição de directrizes gerais no combate à Tuberculose no País, descritas na “Politica e Plano Nacional de CITB em US e ambientes conglomerados de Moçambique”, aprovada em 2010 de implementação a nível nacional.
No intervalo de 2016 até o final de 2018, o Ministério da Saúde formou 412 formadores provinciais em CITB de todas as províncias do país, e foram apoiados a elaboração de dos 238 planos de controlo de infeções para TB (Figura 1) os quais estão disseminados a todos os trabalhadores conforme ilustra a figura abaixo.
Figura 1. Número de US com planos de CITB elaborados e funcionais no país até 2018

Durante a elaboração do plano de CITB, os profissionais de saúde são formados em serviço para garantir o acompanhamento de medidas administrativas, ambientais e de proteção respiratória através do uso do respirador N95. Paralelamente, o MISAU levou a cabo mais de 200 rondas de supervisão e assistência técnica baseado na ferramenta de avaliação de risco para infecção por TB – Dashboard e, como resultado destas rondas 40% das US com plano de CITB alcançaram 80% de desempenho nas medidas de CITB. Estas acções, também permitem estabelecer mecanismos para o rastreio periódico de TB em profissionais de saúde através dos gabinetes de consulta para o profissional de saúde, priorizando aqueles afectos em serviços com maior produção de aerossóis. Neste contexto, nos últimos 3 anos, resultando da vigilância ativa para determinação precoce da infecção por TB em.128 US de 10 províncias, 26,503 profissionais de saúde foram rastreados por TB dos quais 492 foram confirmados TB activa (Figura 2) e arrolados aos cuidados e tratamento.
Figura 2. Número de trabalhadores de saúde confirmados activa TB, 2016-2018

Fonte: Resumo mensal da consulta do profissional reportados pelos supervisores provinciais de SSAT
Actualmente, mais profissionais de saúde estão mais consciencializados em relação a adesão na implementação das medidas de CITB assim como as actividades de rastreio periódico de TB, porém as acções de vigilância de TB em profissionais de saúde tem aumentado e como resultado, mais profissionais de saúde têm oportunidade de serem diagnosticados TB precocemente.
É tempo de juntos acabarmos com a TUBERCULOSE em Moçambique.
Uso de aplicativos para sessões de web-palestras no Núcleo central de Telessaúde MZ
Hoje em dia com a necessidade de se comunicar e ter informação em tempo real abaixo custo, existem vários aplicativos de fácil uso e instalação, que podem ser usados para sessões de videoconferência conectando pessoas de diferentes continentes, países e cidades para tomada de decisão em vários sectores de trabalho.
A seguir citamos alguns aplicativos mais utilizados para videoconferência ou webconferência:
- Skype
- Zoom
- StarLeaf
- Google Hangouts
- Google Meet
- BlueJeans
- Pexip
Estes aplicativos, se tornaram de muito utilidade no quotidiano de profissionais de diversas áreas, contudo existem os mais destacados que são: Skype, Zoom e StarLeaf, estes três (03) conseguiram conquistar várias empresas que tem interesse em reuniões virtuais, evitando deste modo deslocação dos seus profissionais e reduzindo deste modo custos.
Recentemente o Google lançou um novo aplicativo de videoconferência voltado para empresas denominado Meet, que permite participar em reuniões de vídeo em HD, parece ser a mais recente adição à lista de produtos empresariais do Google. O serviço ainda está em processo de desenvolvimento e implantação, por isso, está disponível somente na versão web e para o sistema operacional iOS. No entanto, as versões ainda não estão apresentando as mesmas funcionalidades
De uma forma geral, todos esses aplicativos têm custo zero para seu uso e funcionamento, porém consoante as necessidades técnicas que o utilizador (instituição) pode precisar podem sim acarretar algum custo, como por exemplo, o número de utilizadores durante a sessão, gravação em formato de vídeo dentre outras.
Onde pode ser instalado?
Para além de serem utilizados em computadores laptop e desktop, podem ser usados também em mobiles.
O que é necessário para fazer o uso?
Para fazer uso de qualquer um dos aplicativos mencionados, basta ter uma conta de email, desse modo pode-se aceder em qualquer lugar ou dispositivo (computador ou telemóvel) bastando estar ligado a internet, para o caso concreto do Núcleo de Telessaúde MZ, todos os pontos têm uma conta de email (ex: hospital.gurue@localhost) e a mesma está associada a conta StarLeaf.
Aplicativo utilizado no Núcleo de Telessaúde MZ para webpalestras
Telessaúde em Moçambique ou simplesmente Telessaúde MZ tem usado até então o aplicativo StarLeaf em diversos pontos onde opera e a custo zero, tem ajudado bastante na operacionalização diária na troca de experiência entre os profissionais de saúde em tempo real.
Motivos no uso do StarLeaf no Núcleo
Um dos grandes motivos pelo uso do StarLeaf no Núcleo de TelessaúdeMZ, é simplesmente por permitir a comunicação com o equipamento de videoconferência sem custos, sendo que os restantes mencionados acima, exigem custos adicionais para esta funcionalidade.

Núcleo Central de TelessaúdeMZ em plena sessão com o Hospital Distrital de Chiúre na província de Cabo Delgado usando StarLeaf.